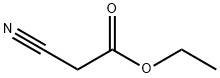
| Apraksts |
Etilciānacetāts ir ciānetiķskābes etilesteris. Etilciānacetāts neitrālos un sārmainos apstākļos ātri hidrolizējas par ciānetiķskābi un etanolu (un tā notiek lielākajā daļā fizioloģisko un vides apstākļu), savukārt skābā pH pussabrukšanas periods ir ievērojami ilgāks.
Tiek ziņots par Knoevenagel etilciānacetāta kondensāciju ar aldehīdu. Ir ziņots par mikroviļņu krāsnī pastiprinātu Knoevenegal etilciānacetāta kondensācijas reakciju ar aldehīdu, P2O5, piperidīnu un hlorbenzolu. |
| Ķīmiskās īpašības |
Etilciānacetāts ir bezkrāsains vai salmu krāsas šķidrums ar maigu patīkamu smaržu |
| Lietojumi |
Etilciānacetātu var izmantot etilglioksilāta sintēzē. To izmantoja, lai izpētītu Knoevenagel kondensācijas reakcijas mikroreaktorā, izmantojot ceolīta katalizatorus, kas iegūti, potējot aminogrupas uz NaX un CsNaX ceolītiem. |
| Lietojumi |
Reaģents, ko izmanto marķētā pirimidīna un purīna sintēzē. Etilciānacetāts ir esteris. To var izmantot etilglioksilāta sintēzē. To izmantoja Knoevenagel kondensācijas reakciju pētīšanai mikroreaktorā, izmantojot ceolīta katalizatorus, kas iegūti, potējot aminogrupas uz NaX un CsNaX ceolītiem. |
| Sagatavošana |
Etilciānacetātu var iegūt, nātrija vai kālija cianīdam iedarbojoties uz etilhloracetātu un nātrija cianīdam iedarbojoties uz nātrija hloracetātu, kam seko esterifikācija. |
| Vispārīgs apraksts |
Bezkrāsains šķidrums. Blīvāks par ūdeni. Saskare var kairināt ādu, acis un gļotādas. Uzliesmošanas temperatūra 210° F. Var būt toksisks norijot. Izmanto citu ķīmisko vielu ražošanai. |
| Gaisa un ūdens reakcijas |
Nedaudz šķīst ūdenī. |
| Reaktivitātes profils |
Etilciānacetāts ir gan nitrils, gan esteris. Esteri reaģē ar skābēm, izdalot siltumu kopā ar spirtiem un skābēm. Spēcīgas oksidējošas skābes var izraisīt spēcīgu reakciju, kas ir pietiekami eksotermiska, lai aizdedzinātu reakcijas produktus. Siltumu rada arī esteru mijiedarbība ar kodīgiem šķīdumiem. Uzliesmojošs ūdeņradis rodas, sajaucot esterus ar sārmu metāliem un hidrīdiem. Nitrili var polimerizēties metālu un dažu metālu savienojumu klātbūtnē. Tie nav saderīgi ar skābēm; nitrilu sajaukšana ar spēcīgām oksidējošām skābēm var izraisīt ārkārtīgi spēcīgas reakcijas. Nitrili parasti nav saderīgi ar citiem oksidētājiem, piemēram, peroksīdiem un epoksīdiem. Bāzu un nitrilu kombinācija var radīt ūdeņraža cianīdu. Nitrilus hidrolizē gan skābē, gan bāzē, iegūstot karbonskābes (vai karbonskābju sāļus). Šīs reakcijas rada siltumu. Peroksīdi pārvērš nitrilus par amīdiem. Nitrili var enerģiski reaģēt ar reducētājiem. Acetonitrils un propionitrils šķīst ūdenī, bet nitriliem, kas ir augstāki par propionitrilu, ir zema šķīdība ūdenī. Tie arī nešķīst ūdens skābēs. |
| Apdraudējums |
Toksisks norijot un ieelpojot. |
| Veselības apdraudējums |
TOKSISKI; ieelpošana, norīšana vai saskare (āda, acis) ar tvaikiem, putekļiem vai vielu var izraisīt smagus savainojumus, apdegumus vai nāvi. Saskare ar izkausētu vielu var izraisīt smagus ādas un acu apdegumus. Reakcijā ar ūdeni vai mitru gaisu izdalīsies toksiskas, kodīgas vai uzliesmojošas gāzes. Reakcija ar ūdeni var radīt daudz siltuma, kas palielinās izgarojumu koncentrāciju gaisā. Uguns izdalīs kairinošas, kodīgas un/vai toksiskas gāzes. Ugunsdzēsības vai atšķaidīšanas ūdens notece var būt kodīga un/vai toksiska un izraisīt piesārņojumu. |
| Ugunsbīstamība |
Uzliesmojošs materiāls: var degt, bet viegli neaizdegas. Viela reaģēs ar ūdeni (daži spēcīgi), izdalot uzliesmojošas, toksiskas vai kodīgas gāzes un noteci. Sildot, tvaiki var veidot sprādzienbīstamus maisījumus ar gaisu: telpās, ārā un kanalizācijas sprādzienbīstamība. Lielākā daļa tvaiku ir smagāki par gaisu. Tie izplatīsies pa zemi un sakrājas zemās vai norobežotās vietās (kanalizācijā, pagrabos, tvertnēs). Tvaiki var nokļūt līdz aizdegšanās avotam un uzliesmot atpakaļ. Saskaroties ar metāliem, var izdalīties uzliesmojoša ūdeņraža gāze. Karsējot vai piesārņojot ar ūdeni, tvertnes var eksplodēt. |
| Drošības profils |
oison, norijot. Vidēji toksisks intraperitoneāli un subkutāni. Uzliesmojošs, ja tiek pakļauts karstumam vai liesmai; var reaģēt ar oksidējošiem materiāliem. Wdl reaģē ar ūdeni vai tvaiku, veidojot toksiskus un viegli uzliesmojošus tvaikus. Ugunsgrēka dzēšanai izmantojiet CO2, sauso ķimikāliju. Karsējot līdz sadalīšanās brīdim vai saskaroties ar skābi vai skābiem dūmiem, tas izdala ļoti toksiskus CN- dūmus. Skatīt arī NITRILI. |
| Iespējama iedarbība |
Nitrils, ko izmanto krāsvielu, farmaceitisko līdzekļu un citu ķīmisko vielu ražošanai. |
| Pirmā palīdzība |
Ja šī ķimikālija nokļūst acīs, nekavējoties izņemiet visas kontaktlēcas un nekavējoties skalojiet vismaz 15 minūtes, laiku pa laikam paceļot augšējo un apakšējo plakstiņu. Nekavējoties meklēt medicīnisko palīdzību. Ja šī ķīmiskā viela nonāk saskarē ar ādu, novelciet piesārņoto apģērbu un nekavējoties nomazgājiet ar ziepēm un ūdeni. Nekavējoties meklēt medicīnisko palīdzību. Ja šī ķīmiskā viela ir ieelpota, izņemiet no iedarbības vietas, sāciet elpošanu (izmantojot vispārējus piesardzības pasākumus, tostarp reanimācijas masku), ja elpošana ir apstājusies, un CPR, ja sirds darbība ir apstājusies. Nekavējoties pārsūtiet uz medicīnas iestādi. Kad šī ķīmiskā viela ir norīta, meklējiet medicīnisko palīdzību. Dodiet lielu daudzumu ūdens un izraisiet vemšanu. Personai bezsamaņā neizraisīt vemšanu |
| uzglabāšana |
re indes vieta. Pirms sākat strādāt ar šo ķīmisko vielu, jums jāapmāca, kā pareizi rīkoties un uzglabāt to. Uzglabāt cieši noslēgtos konteineros vēsā, labi vēdināmā vietā, prom no oksidētājiem, stiprām bāzēm, stiprām skābēm, reducētājiem, mitruma un aizdegšanās avotiem. Ja iespējams, automātiski sūknējiet šķidrumu no mucām vai citiem uzglabāšanas konteineriem, lai apstrādātu konteinerus. |
| Piegāde |
UN3276 Nitrili, šķidri, toksiski, nos, bīstamības klase: 6.1; Etiķetes: 6.1-Indīgi materiāli, nepieciešams tehniskais nosaukums, iespējama ieelpošanas bīstamība (5. īpašais noteikums). |
| Attīrīšanas metodes |
Esteri vairākas reizes sakratiet ar 10% Na2CO3 ūdens šķīdumu, labi nomazgājiet ar ūdeni, nosusiniet ar Na2SO4 un frakcionēti destilējiet. [Beilstein 2 IV 1889.] |
| Nesaderības |
Nesaderīgs ar oksidētājiem (hlorāti, nitrāti, peroksīdi, permanganāti, perhlorāti, hlors, broms, fluors utt.); saskare var izraisīt aizdegšanos vai sprādzienu. Sargāt no sārmainiem materiāliem, stiprām bāzēm, stiprām skābēm, oksoskābēm, epoksīdiem un reducētājiem. Nitrili var polimerizēties metālu un dažu metālu savienojumu klātbūtnē. Tie nav saderīgi ar skābēm; nitrilu sajaukšana ar spēcīgām oksidējošām skābēm var izraisīt ārkārtīgi spēcīgas reakcijas. Nitrili parasti nav saderīgi ar citiem oksidētājiem, piemēram, peroksīdiem un epoksīdiem. Bāzu un nitrilu kombinācija var radīt ūdeņraža cianīdu. Nitrilus hidrolizē gan skābē, gan bāzē, iegūstot karbonskābes (vai karbonskābju sāļus). Šīs reakcijas rada siltumu. Peroksīdi pārvērš nitrilus par amīdiem. Nitrili var enerģiski reaģēt ar reducētājiem. Acetonitrils un propionitrils šķīst ūdenī, bet nitriliem, kas ir augstāki par propionitrilu, ir zema šķīdība ūdenī. Tie arī nešķīst ūdens skābēs. Reaģē ar mitrumu, ūdeni un tvaiku, veidojot toksiskus izgarojumus. |
| Atkritumu likvidēšana |
Konsultējieties ar vides regulējošām aģentūrām, lai saņemtu norādījumus par pieņemamu utilizācijas praksi. Atkritumu radītājiem, kas satur šo piesārņotāju (lielāks par vai vienāds ar 100 kg/mēn.), ir jāatbilst EPA noteikumiem, kas regulē uzglabāšanu, transportēšanu, apstrādi un atkritumu apglabāšanu. |