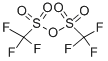
| Apraksts |
Trifluormetānsulfonanhidrīds, kas pazīstams arī kā trifluorskābes anhidrīds, ir izrādījies ārkārtējs reaģents plaša spektra transformācijām. Kā komerciāli un viegli pieejams reaģents, tas ir plaši izmantots sintētiskajā ķīmijā tā augstās elektrofilitātes dēļ. Ņemot vērā tā augsto afinitāti pret O-nukleofīliem, reakcija ar spirtiem, karbonilgrupām, sēra fosfora un joda oksīdiem, veidojot atbilstošos triflātus, ir ļoti labvēlīga. Kā viena no vadošajām grupām organiskajā ķīmijā, radītie triflāti paver durvis dažādām pakārtotām transformācijām, tostarp (bet ne tikai) aizvietošanas reakcijām, šķērssavienojuma procesiem, redoksreakcijām un pārkārtojumiem[1-2] . |
| Ķīmiskās īpašības |
dzidrs bezkrāsains līdz gaiši brūns šķidrums |
| Lietojumi |
Trifluormetānsulfonanhidrīds ir spēcīgs elektrofils, ko izmanto ķīmiskajā sintēzē triflilgrupas ievadīšanai. |
| Lietojumi |
Trifluormetānsulfonanhidrīdu izmanto, lai fenolus un imīnu pārveidotu par trifluoresteru un NTf grupu. Tas ir spēcīgs elektrofils, ko izmanto triflilgrupas ieviešanai ķīmiskajā sintēzē. Tas kalpo kā reaģents alkil- un viniltriflātu pagatavošanā, kā arī mannosazīda metiluronāta donoru stereoselektīvai sintēzei. Tas darbojas kā katalizators glikozilēšanai ar anomēriem hidroksicukuriem, lai iegūtu polisaharīdus. |
| Definīcija |
ChEBI: Triflic anhidrīds ir organosulfonanhidrīds. Tas ir funkcionāli saistīts ar triflskābi. |
| Reaktivitātes profils |
Terciāro un sekundāro amīdu elektrofilā aktivācija ar trifluorskābes anhidrīdu (Tf2O; rifluormetānsulfonanhidrīds) vieglos apstākļos rada attiecīgi imīnija un iminotriflātus, kurus var izmantot kā daudzpusīgus reaģentus, lai reaģētu ar dažādiem C-, N-, O- un S. -nukleofīli amīda funkcijas pārveidošanai dažādos produktos. Citi skābekli saturoši nukleofīli, piemēram, sulfoksīdi un fosfora oksīdi, arī varētu tikt pakļauti nukleofīlam uzbrukumam ar Tf2O, lai radītu tionija triflātu, elektrofīlās P-sugas un fosfonija triflātu. Šīs ļoti aktīvās pārejošās sugas varētu viegli iziet nukleofīlas aizvietošanas reakcijas turpmākām daudzveidīgām transformācijām. Turklāt spēcīgās elektrofilās īpašības dēļ Tf2O ir tendence reaģēt ar salīdzinoši vājiem nukleofīliem, piemēram, nitrila grupām vai dažiem slāpekli saturošiem heterocikliskiem savienojumiem. Turklāt Tf2O ir izmantots arī kā efektīvs radikāļu trifluormetilēšanas un trifluormetiltiolēšanas reaģents, izdalot SO2 vai deoksigenācijas procesā trifluormetilētu un trifluormetiltiolētu savienojumu sintēzei[2]. |
| Apdraudējums |
Var būt kodīgs metāliem. Kaitīgs norijot. Izraisa smagus ādas apdegumus un acu bojājumus. |
| Uzliesmojamība un sprādzienbīstamība |
Nav klasificēts |
| Sintēze |
Trifluormetānsulfonanhidrīda sintēze ir šāda:
Sausā, {{0}} ml, apaļkolbā iepilda 36,3 g. (0,242 mol) trifluormetānsulfonskābes (1. piezīme) un 27,3 g. (0,192 moli) fosfora pentoksīda (2. piezīme). Kolbu aizver ar aizbāzni un ļauj nostāvēties istabas temperatūrā vismaz 3 stundas. Šajā periodā reakcijas maisījums mainās no vircas uz cietu masu. Kolba ir aprīkota ar īsceļa destilācijas galviņu un vispirms tiek karsēta ar karsta gaisa plūsmu no karstuma pistoles un pēc tam ar liesmu no neliela degļa.Kolbu karsē, līdz vairs nedestilējas trifluormetānsulfonanhidrīds, bp 82–115 grādi, iegūstot 28,4–31,2 g. (83–91%) anhidrīda, bezkrāsains šķidrums. Lai gan šis produkts ir pietiekami tīrs lietošanai nākamajā darbībā, atlikušo skābi var noņemt no anhidrīda, izmantojot šādu procedūru. Suspensija 3,2 g. fosfora pentoksīda 31,2 g. neattīrīta anhidrīda maisa istabas temperatūrā kolbā ar aizbāzni 18 stundas. Pēc tam, kad reakcijas kolba ir aprīkota ar īsceļa destilācijas galvu, to karsē eļļas vannā, iegūstot 0,7 g. no priekšpuses, bp 74–81 grāds, kam seko 27,9 g. tīra trifluormetānsulfonskābes anhidrīda, bp 81–84 grādi.

|
| uzglabāšana |
Uzglabāt vēsā, sausā, labi vēdināmā vietā. Mitruma jutīgs. |
| Attīrīšanas metodes |
To var svaigi pagatavot no bezūdens skābes (11,5 g) un P2O5 (11,5 g jeb puse no šī svara), atstājot istabas temperatūrā uz 1 stundu, destilējot gaistošos produktus, pēc tam destilējot caur īsu Vigreux kolonnu. To viegli hidrolizē H2O, un pēc dažām dienām tas ievērojami sadalās, atbrīvojot SO2 un veidojot viskozu šķidrumu. Glabājiet to sausā temperatūrā zemā temperatūrā. [Bērdons et al. J Chem Soc 2574 1957, Beard et al. J Org Chem 38 373 1973, Beilstein 3 IV 35.] |
| Atsauces |
[1] Haokji Džan. "Trifluormetānsulfonanhidrīds amīdu aktivācijā: spēcīgs instruments heterociklisko serdeņu kalšanai." TCIMAIL (2021).
[2] Dr. Qixue Qin, prof. Dr. Ning Jiao, Zengrui Cheng. "Pēdējie trifluormetānsulfonanhidrīda pielietojumi organiskajā sintēzē." Angewandte Chemie 135 10 (2022). |