Produkta ievads
| 2,2,2-Trifluoretanols Pamatinformācija |
| Apraksts Ķīmiskās īpašības Izmantošana Sagatavošanas metode Bīstamības un drošības informācija |
| Produkta nosaukums: | 2,2,2-trifluoretanols |
| Sinonīmi: | Trifluoretanols(L);2,2,2-trifluoretanols,trifluoretilspirts;2,2,2-trifluoretanols, reaģenta pakāpe;2,2,2-trifluoretāns;2,2,{ {11}}Trifluoretanols-1-99%;2-Hidroksi-1,1,1-trifluoretāns, (trifluormetil)metanols;2,2,2-TRIFLUOROETANOLS -D3, AUGSTS BAGĀTINĀJUMS; 1,2,2-trifluoretanol-1- |
| CAS: | 75-89-8 |
| MF: | C2H3F3O |
| MW: | 100.04 |
| EINECS: | 200-913-6 |
| Produktu kategorijas: | fluororganiskie savienojumi; organiskās vielas; API starpprodukti; citi reaģenti; fluorēti celtniecības bloki; fluorēšanas reaģenti un fluorētu bioķīmisko savienojumu celtniecības bloki; sintētiskā organiskā ķīmija; ķīmija; 3; 1; bc0001; R00001 |
| Mol fails: | 75-89-8.mol |
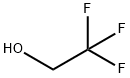 |
|
| 2,2,2-Trifluoretanola ķīmiskās īpašības |
| Kušanas punkts | -44 grādi (lit.) |
| Vārīšanās temperatūra | 77-80 grāds (lit.) |
| blīvums | 1,391 g/ml 20 grādu temperatūrā |
| tvaika blīvums | 3,5 (pret gaisu) |
| tvaika spiediens | 70 mm Hg (25 grādi) |
| refrakcijas indekss | n20/D 1,3 (lit.) |
| Fp | 85 grādi F |
| uzglabāšanas temp. | Uzglabāt zem +30 grādu. |
| šķīdība | šķīst hloroformā, metanolā |
| pka | 12,4 (pie 25 grādiem) |
| formā | Šķidrums |
| krāsa | Dzidrs bezkrāsains |
| Īpatnējais smagums | 1.373 |
| Smarža | Alkohola smaka |
| PH diapazons | 5-7 (10% aq soln) |
| sprādzienbīstamības robeža | 8.4-28.8%(V) |
| Šķīdība ūdenī | Sajaucas ar ūdeni, ēteriem, ketoniem, spirtiem un hloroformu. |
| λmaks | λ: 260 nm Maksimālais: mazāks vai vienāds ar 0,03 λ: 280 nm Maksimālais: mazāks vai vienāds ar 0,02 |
| Merck | 14,9682 |
| BRN | 1733203 |
| Dielektriskā konstante | 8.5500000000000007 |
| Stabilitāte: | Stabils. Uzliesmojošs – ievērojiet plašas sprādzienbīstamības robežas. Mitruma jutīgs. Nesaderīgs ar spēcīgiem oksidētājiem, stiprām skābēm, nātriju, kāliju. |
| InChIKey | RHQDFWAXVIIEBN-UHFFFAOYSA-N |
| CAS datu bāzes atsauce | 75-89-8(CAS datu bāzes atsauce) |
| NIST ķīmijas atsauce | Etanols, 2,2, 2-trifluor-(75-89-8) |
| EPA vielu reģistra sistēma | 2,2,2-Trifluoretanols (75-89-8) |
| Drošības informācija |
| Bīstamības kodi | Xn, T, F |
| Riska paziņojumi | 10-20/21/22-37/38-41-62-38-36/37/38 |
| Drošības paziņojumi | 26-36-39-45-36/37/39-16 |
| RIDADR | ANO 1986 3/PG 3 |
| WGK Vācija | 1 |
| RTECS | KM5250000 |
| Pašaizdegšanās temperatūra | ~896 grādi F |
| Bīstamības piezīme | Uzliesmojošs/toksisks |
| TSCA | Jā |
| Bīstamības klase | 3 |
| Iepakojuma grupa | III |
| HS kods | 29055910 |
| Toksiskums | LD50 iekšķīgi trušiem: 240 mg/kg LD50 dermāli žurkām 1680 mg/kg |
| MSDS informācija |
| Pakalpojumu sniedzējs | Valoda |
|---|---|
| 2,2,2-trifluoretanols | angļu valoda |
| ACROS | angļu valoda |
| SigmaAldrihs | angļu valoda |
| ALFA | angļu valoda |
| 2,2,2-Trifluoretanola lietošana un sintēze |
| Apraksts | 2,2,2-trifluoretanolu vai trifluoretanolu sauc par TFEA vai TEF, tas ir svarīgs fluoru saturošas alifātiskās vielas starpprodukts, tas ir bezkrāsains, tas ir šķidrums, kas sajaucas ar ūdeni, tam ir līdzīga smarža kā etanolam. Sakarā ar trifluormetila spēcīgo elektronu izvadīšanas efektu, trifluormetilskābe ir spēcīgāka par etanolu, tā var radīt ar ūdeņradi saistītu stabilu kompleksu (piemēram, tetrahidrofurānu, piridīnu) ar heterociklisku savienojumu. Pateicoties šīm unikālajām fizikālajām un ķīmiskajām īpašībām un īpašajai molekulārajai struktūrai, tam ir atšķirīga veiktspēja ar citiem spirtiem, tas var piedalīties dažādās organiskās reakcijās, to var oksidēt par acetaldehīda trifluormetilskābi vai trifluoretiķskābi, tas var arī nodrošināt trifluormetilu, tas var piedalīties Still-Gennari Horner-Wadsworth-Emmons reakcijas uzlabojumos. To plaši izmanto medicīnā, pesticīdos, krāsvielas, enerģētikā un citos organiskās sintēzes aspektos. Galvenais trifluoretanola lietojums ir kā anestēzijas līdzeklis, agrākais fluora acetilēna ēteris, ko sintezē trifluoretanols un acetilēns, novērš lielākas broma-fluoralkānu blakusparādības kā anestēzijas līdzekli, un pēc tam trihloretanolu izmanto kā izejvielu, lai izveidotu neuzliesmojošu, zemas toksicitātes izoflurāna alkāni un jaunā hlorfluoralkāna anestēzijas augstā veiktspēja. Trifluoretanolu var ievadīt zāļu struktūrā kā funkcionālās grupas trifluormetilgrupu, tas var radīt ievērojamu fizioloģisko aktivitāti, palielināt taukos šķīstošo molekulu daudzumu, uzlabot efektivitāti vai samazināt organisma blakusparādības, tā sintētiskajām zālēm ir centrālo nervu sistēmu stimulanti flutikazons Seula, aizvietotie piridīni kuņģa citoplazmas protonu sūkņa inhibitori Lansoprazols un Pariprazols, antiaritmiski līdzekļi flekainīds ar amīniem un pretsāpju līdzekļi benzodiazepīni un dizūrijas ārstēšana KMD-3212 un tā tālāk. |
| Ķīmiskās īpašības | Vārīšanās temperatūra ir 73,6 grādi, kušanas temperatūra ir -43,5 grādi, laušanas koeficients ir 1,2940, blīvums (25 grādi) ir 1,383 g/cm3, iztvaikošanas entalpija ir 37,8 kJ/mol. |
| Lietojumi | (1) To var izmantot kā trifluoretil- un trifluoretiķskābes etoksikarbonila aģenta, sintētisko narkotiku fluorīda ētera (fluoroksēna), izoflurāna (izoflurāna) un hlora halotāna (desflurāna), centrālās nervu sistēmas stimulatoru flutikazona Seula (Flowotyl), protonu sūkņa inhibitora importa līdzekli. lansoprazols (Lansoprazols, pp inhibitori), antiaritmiski līdzekļi flekainīds ar amīnu (Flecamide), pretsāpju līdzekļi, benzodiazepīni (Quazepam), apgrūtināta urinēšana terapeitiskais līdzeklis KMD-3213, herbicīds trifluormetiltiometils (Triflusulfuronmethyl). (2) To var izmantot ķīmiskiem reaģentiem. (3) To var izmantot kā šķīdinātāju, to var izmantot kā trifluoretilēna un trifluoretiķskābes etoksikarbonila aģenta importa līdzekli, to var izmantot arī kā farmaceitiskus, pesticīdu starpproduktus. (4) To var izmantot kā šķīdinātāju, to izmanto arī kā zāles, pesticīdu starpproduktus. |
| Sagatavošanas metode | Kopš 1933. gada Swarts kā izejvielu izmantoja trifluoretiķskābes anhidrīdu, trihloretanola iegūšanai izmantoja katalītiskās reducēšanas metodi, esam izstrādājuši virkni sintētisko metožu. Atkarībā no veida reakcijas var iedalīt trīs veidos: oksidēšana, reducēšana un hidrolīze. Pēc izejvielām to var iedalīt trifluoretiķskābes metodē, trifluoracetilhlorīda metodē, trifluoretiķskābes anhidrīda metodē, trifluoracetāta likumā, trifluoretiķskābes acetaldehīdā, polivinilidēnfluorīda metodē, trifluoretāna (HFC-143a) metodē un trifluorhloretāna (HCFC{{2}) metodē. }}a) metode. |
| Informācija par apdraudējumiem un drošību | Kategorija:Uzliesmojošs šķidrums Toksicitātes klasifikācija:ļoti toksisks Akūta perorāla toksicitāte – žurkas LD50:240 mg/kg; Oral-Mouse LD50: 366 mg/kg Dati par kairinājumu:Āda-Trusis 0,75 mg/24 stundās un smagi; Acis-truša 20 mg/24 h viegls Uzliesmojamības bīstamības raksturojums:Saskaroties ar uguni, karstumu, oksidētājiem, tas ir uzliesmojošs; tas var sadegt un radīt toksiskus fluora izgarojumus. Uzglabāšanas īpašības:Valsts kases ventilācijas žāvēšana zemā temperatūrā; tas jāuzglabā atsevišķi ar oksidētājiem. Ugunsdzēšanas līdzeklis:Sausais pulveris, sausas smiltis, oglekļa dioksīds, putas, 1211 ugunsdzēsības līdzeklis. |
| Ķīmiskās īpašības | Bezkrāsains šķidrums |
| Lietojumi | Medicīnisko anestēzijas līdzekļu, farmaceitisko līdzekļu un agroķīmisko vielu sintēzē; polimerizācijās. Olbaltumvielu denaturants; stabilizē peptīdu struktūras. Tīrīšanas šķīdinātājs; eluents HPLC separācijās; darba šķidrums Rankine siltuma cikla sistēmās. Videi draudzīga alternatīva CFC. |
| Lietojumi | Trifluoretanols kalpo kā šķīdinātājs un izejviela organiskajā ķīmijā un bioloģijā. TFE ir izvēlēts šķīdinātājs ūdeņraža peroksīda izraisītai sulfīdu oksidēšanai. Trifluoretanols darbojas kā proteīnu denaturants. To izmanto noteiktu farmaceitisko un zāļu vielu ražošanā. Zāļu fluormērs, kas ir 2,2,2-trifluor-1-viniloksietāns, ir trifluoretanola vinilēteris. Tas ir efektīvs šķīdinātājs peptīdiem un proteīniem, un to izmanto uz NMR balstītiem proteīnu locīšanas pētījumiem un neilona ražošanā. Kā trifluormetilgrupas avots to izmanto vairākās organiskās reakcijās, piemēram, Still-Gennari modifikācijā Hornera-Vadsvorta-Emonsa reakcijas (HWE) reakcijā. |
| Lietojumi | 2,2,2-Trifluoretanolu (trifluoretilspirtu, TFE) izmanto, lai pētītu proteīnu konformācijas stāvokļus un proteīnu locīšanas pārlocīšanas procesus. |
| Definīcija | ChEBI: 2,2,2-trifluoretanols ir fluora spirts. Tas ir funkcionāli saistīts ar etanolu. |
| Drošības profils | Saindē, norijot, intravenozi un intraperitoneāli. Vidēji toksisks ieelpojot un saskaroties ar ādu. Eksperimentālā reproduktīvā ietekme. Spēcīgs ādas un acu kairinājums. Karsējot līdz sadalīšanai, tas izdala toksiskus F- izgarojumus. |
| Attīrīšanas metodes | Nosusiniet to ar CaSO4 un nedaudz NaHCO3 (lai noņemtu skābes pēdas) un destilējiet. Ļoti TOKSISKI tvaiki. [Beilstein 1 IV 1370.] |
| 2,2,2-Trifluoretanola sagatavošanas produkti un izejvielas |
| Izejvielas | 2,2,2-Trifluorodiazoethane-->Benzene, [(2,2,2-trifluoroethoxy)methyl]--->4-(prop-1-en-2-il)fenilacetāts |
| Sagatavošanas produkti | 2-Chloromethyl-3-methyl-4-(2,2,2-trifluoroethoxy)pyridine hydrochloride-->6-(2,2,2-TRIFLUOROETHOXY)NICOTINIC ACID-->2-(2,2,2-TRIFLUOROETHOXY)PYRIDINE-3-CARBOXYLIC ACID-->TRIS(2,2,2-TRIFLUOROETHYL)PHOSPHATE-->TRIFLUOROACETALDEHYDE HYDRATE-->3,3,3-Trifluoropropionic acid-->Isoflurane-->1,1,1,2-Tetrafluoroethane-->2-CHLORO-1,1,1-TRIFLUOROETHANE-->pent-1-en-3-yne-->1,3,2-Dioxaphospholane, 2-(2,2,2-trifluoroethoxy)-, 2-oxide-->2-Hydroxy-1,3,2-dioxaphospholane 2-oxide-->2,6-BIS(2,2,2-TRIFLUOROETHOXY)BENZONITRILE-->2,2,2-TRIFLUOROETHYL CHLOROFORMATE-->1,1,2,3,3,3-HEXAFLUOROPROPYL 2,2,2-TRIFLUOROETHYL ETHER-->Kālija trifluoracetāts |
Populāri tagi: 2,2,2-trifluoretanols, Ķīna 2,2,2-trifluoretanola ražotāji, piegādātāji, rūpnīca
Pāri: 2,2-Difluoretanols
Nākamo: Bromoetiķskābe
Jums varētu patikt arī
Nosūtīt pieprasījumu




![3,9-divinil-2,4,8,10-tetraoksaspiro[5.5]undekāns](/uploads/41226/small/3-9-divinyl-2-4-8-10-tetraoxaspiro-5-59a6ae.gif?size=336x0)