
Produkta ievads
| Tetrabutilamonija bromīds Pamatinformācija |
| Fizikālās un ķīmiskās īpašības Pielietojums Lietojumi preparāts Toksicitāte |
| Produkta nosaukums: | Tetrabutilamonija bromīds |
| Sinonīmi: | 1-Butānamīns, N,N,N-tributil-, bromīds;1-Butānamīns,N,N,N-tributil-,bromīds;n,n,n-tributil-1-butānamīnibromīds; ALIQUAT(R) 100; IPC-TBA-BR; tetrabutilazāna bromīds; tetrabutilamīnija bromīds; tetrabutilamonija bromīds, 99%, jonu pāru hromatogrāfijai |
| CAS: | 1643-19-2 |
| MF: | C16H36BrN |
| MW: | 322.37 |
| EINECS: | 216-699-2 |
| Produktu kategorijas: | Organo amīnu halogenīds;Citi produkti;Amonija sāļi Būtiskas ķimikālijas;Reaģents Plus;Ikdienas reaģenti;Amonija sāļiAnalītiskie reaģenti;Elektroķīmija;Atbalstošie elektrolīti elektroķīmijai;Anjonu HPLC;Chromatography/CE Reagents; jonu; jonu pāris Reaģenti - anjonu koncentrāts; ceturtdaļas amonija sāļi; amonija bromīdi (kvartārais); analītiskā ķīmija; HPLC jonu pāru reaģenti skābiem paraugiem; jonu pāru reaģenti HPLC; kvartāra amonija savienojumi; amonijs, sulfonijs (likinijs, fosforijs); Šķidrumi;Sintētiskā organiskā ķīmija;Amonija sāļi;zaļākas alternatīvas: katalīze;fāzes pārneses katalizatori;farmaceitiskie starpprodukti;1643-19-2;bc0001 |
| Mol fails: | 1643-19-2.mol |
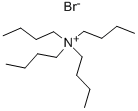 |
|
| Tetrabutilamonija bromīda ķīmiskās īpašības |
| Kušanas punkts | 102-106 grāds (lit.) |
| Vārīšanās punkts | 102 grādi |
| blīvums | 1,039 g/ml 25 grādu temperatūrā |
| tvaika spiediens | 0Pa pie 25 grādiem |
| refrakcijas indekss | n20/D 1.422 |
| Fp | 100 grādi |
| uzglabāšanas temp. | Uzglabāt zemāk par +30 grādu. |
| šķīdība | H2O: 0,1 g/mL, dzidrs, bezkrāsains |
| formā | Kristālisks pulveris |
| pka | 0[20 grādos ] |
| Īpaša gravitāte | 1.007 |
| krāsa | Balts līdz nedaudz krēmkrāsas |
| Smarža | Amīns līdzīgs |
| PH | 3,5 līdz 7.0 (50 g/l, 25 grādi) |
| Šķīdība ūdenī | 600 g/L (20 ºC) |
| Jūtīgs | Higroskopisks |
| λmaks | λ: 240 nm Maksimālais: 0,04 λ: 250 nm Maksimālais: 0,03 λ: 260 nm Maksimālais: 0,02 λ: 500 nm Maksimālais: 0,02 |
| BRN | 3570983 |
| Stabilitāte: | Stabils. Nesaderīgs ar spēcīgiem oksidētājiem. Sargāt no mitruma. |
| InChIKey | JRMUNVKIHCOMHV-UHFFFAOYSA-M |
| LogP | 0.839 25 grādos |
| CAS datu bāzes atsauce | 1643-19-2(CAS datu bāzes atsauce) |
| NIST ķīmijas atsauce | Tetra-N-butilamonija bromīds (1643-19-2) |
| EPA vielu reģistra sistēma | Tetrabutilamonija bromīds (1643-19-2) |
| Drošības informācija |
| Bīstamības kodi | Xi, Xn |
| Riska paziņojumi | 36/37/38-22 |
| Drošības paziņojumi | 26-36-37/39 |
| WGK Vācija | 3 |
| F | 3 |
| Bīstamības piezīme | Kairinošs |
| TSCA | Jā |
| HS kods | 29239000 |
| MSDS informācija |
| Pakalpojumu sniedzējs | Valoda |
|---|---|
| Tetrabutilamonija bromīds | Angļu |
| ACROS | Angļu |
| SigmaAldrihs | Angļu |
| ALFA | Angļu |
| Tetrabutilamonija bromīda lietošana un sintēze |
| Fizikālās un ķīmiskās īpašības | Tetrabutilamonija bromīds, pazīstams arī kā tetrabutilamonija bromīds. Balts kristāls, šķīsts. 118 grādu kušanas temperatūra. Šķīst ūdenī, spirtā, ēterī un acetonā, nedaudz šķīst benzolā.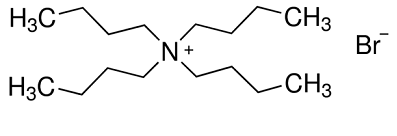 1. attēls: tetrabutilamonija bromīda strukturālā formula |
| Pieteikums | (1) Izmanto kā reaģentu organiskās sintēzes analīzei. (2) Tetrabutilamonija bromīds ir arī efektīvs fāzes pārneses katalizators. Fāzes pārneses katalizators, saukts par PTC, spēj pārnest ūdens fāzi (vai organisko fāzi) uz organiskās fāzes (vai ūdens fāzes) katalizatoru, kas var izraisīt reakciju starp ūdens fāzi un katalizatora organisko fāzi. PTC funkcija ir mainīt jonu šķīdināšanas pakāpi, palielināt jonu reakcijas aktivitāti, paātrināt reakcijas ātrumu un tā tālāk. Atrisināt problēmu pagātnē divās reakcijas fāzēs ir grūti reaģēt. Parastie ceturtā amonija sāls fāzes pārneses katalizatori ir: benziltrietilamonija hlorīds, trioktila metilamonija hlorīds, tetrametilamonija bromīds, tetrapropilamonija hlorīds, tetrabutilamonija bromīds, tetrabutilamonija trietiljodīds, helocilbenziljodīds iltrietilamonija bromīds. Fāzes pārneses katalizators tiek plaši izmantots organiskajā sintēzē: R2C savienojumu (karbēna tipa savienojuma) iegūšanai, tālākai atbilstošo nitrila, izonitrila, halona, dihlormetāna ciklopropāna atvasinājumu, hidroksi skābju un diazometāna sagatavošanai. Alkilēšanas reakcijai, salīdzinot ar tradicionālajām metodēm, lai izvairītos no skarbajiem sausas darbības apstākļiem un lielas ražības, to var izmantot arī redoksreakcijā, estera hidrolīzē, aizvietošanas reakcijā, kondensācijas reakcijā, pievienošanas reakcijā, polimerizācijas reakcijā, pievienošanas reakcijā. oglekļa un reakcijas likvidēšana utt. (3) Organiskās sintēzes starpproduktiem fāzes pārneses katalizators (4) Jonu savienošanas reaģenti bakampicilīna, sultamicilīna līdzīgo sintēzei. (5) Jonu pāru hromatogrāfijas reaģenti, fāzes pārneses katalizators. Bakampicilīnam, sultamicilīnam līdzīga sintēze. |
| Lietojumi | Tetrabutilamonija bromīds (TBAB) ir kvartāra amonija savienojums. Tas ir visplašāk izmantotais fāzes pārneses katalizators. Tā saskarnes īpašības ir pētītas hidroksīda izraisītu reakciju gadījumā. To var izmantot, lai izprastu fāzes pārneses reakciju mehānismu. Tiek ziņots, ka TBAB samazina aiztures laiku un noņem pīķa astes, darbojoties kā jonu pāru reaģents kvartārā amonija savienojumu hromatogrāfiskās analīzes laikā. Izkausētā stāvoklī TBAB uzvedas kā jonu šķidrums, kas ir daudzsološa zaļa alternatīva organiskajiem šķīdinātājiem organiskajā sintēzē. Ir noteikta tā molārā siltumietilpība, entropija un brīvās enerģijas funkcija. Nesen izkausēts tetrabutilamonija bromīds (TBAB) tika izmantots kā zemi toksisks un rentabls IL vairākās konstruktīvās sintētiskās transformācijās. Tetrabutilamonija bromīdu (TBAB) var izmantot kausētā stāvoklī šādos procesos: (2S)-5-(3-fenil-2-ftalimidilpropanoilamino)izoftalskābes sintēze. Alkil-aizvietotu pirolu sintēze bez katalizatora un organiskā šķīdinātāja. Ditioacetālu sintēze no acetāļiem, izmantojot transtioacetalizāciju vidē, kurā nav šķīdinātāju. Poliamīdu (PA) sintēze, polimerizējot tereftalskābi un diizocianātus. Katalizējiet tiolu pievienošanu konjugētajiem alkēniem. Polivinilhlorīda dehidrohlorēšana. |
| sagatavošana | Sagatavošanas metodes: ir pieejamas vairākas metodes, lai efektīvi atgūtu kvaternāro amonija jonu. Sagatavots tri-n-butilamīna un n-butilbromīda reakcijā. |
| Toksiskums | Akūts perorāls LD50 (pele): 590 mg/kg. Ieelpošana, norīšana un saskare ar ādu toksisks ādai, acīm un elpošanas sistēmas kairinājums. Plašāka informācija no ChemicalBook Xiaonan redaktora (2015-09-16). |
| Ķīmiskās īpašības | balti kristāli vai pulveris |
| Lietojumi | Tetrabutilamonija bromīds tiek izmantots polimēru saules bateriju sintēzē. Izmanto arī vienkomponentu zaļo gaismu izstarojošo elektroķīmisko elementu sintēzē. |
| Definīcija | ChEBI: Tetrabutilamonija bromīds ir tetrabutilamonija sāls ar bromīdu kā anjonu ekvivalentu. Tas ir organiskā bromīda sāls un tetrabutilamonija sāls. |
| ieguvumi | Tetrabutilamonija bromīds ir videi nekaitīgs, negaistošs, neuzliesmojošs, nekodīgs, lēts, komerciāli pieejams amonija sāls ar augstu termisko un ķīmisko stabilitāti. TBAB tetrabutilamonija sāls var izšķīst gan ūdens, gan organiskos šķīdinātājos, kas palīdz transportēt ūdenī šķīstošos anjonus reaģentus organiskajā fāzē. Turklāt izkausētais TBAB tika izmantots arī kā efektīvs jonu šķidrums, lai veiktu organiskās pārvērtības bez šķīdinātājiem [1]. |
| Vispārīgs apraksts | Tetrabutilamonija bromīds, kvartāra amonija savienojums, ko plaši izmanto kā fāzes pārneses katalizatoru. TBAB samazina aiztures laiku un noņem pīķa astes, darbojoties kā jonu pāru reaģents kvartārā amonija savienojumu hromatogrāfiskās analīzes laikā. Izkausētā stāvoklī TBAB uzvedas kā jonu šķidrums, kas ir daudzsološa zaļa alternatīva organiskajiem šķīdinātājiem polimēru sintēzē. |
| Uzliesmojamība un sprādzienbīstamība | Nav klasificēts |
| Attīrīšanas metodes | Kristalizējiet sāli no *benzola (5mL/g) 80o temperatūrā, pievienojot karstu n-heksānu (trīs tilpumi) un ļaujot atdzist. Nosusiniet to virs P2O5 vai Mg(ClO4)2 vakuumā. Sāls ir ļoti higroskopiska. To var arī kristalizēt no etilacetāta vai sausa acetona, pievienojot dietilēteri un žāvēt vakuumā 60o temperatūrā 2 dienas. Tas ir kristalizēts no acetona, pievienojot dietilēteri. Tas ir tik higroskopisks, ka visas manipulācijas jāveic sausā kastē. Tas ir attīrīts, izgulsnējot no piesātināta šķīduma sausā CCl4, pievienojot cikloheksānu vai pārkristalizējot no etilacetāta, pēc tam karsējot vakuumā līdz 75o P2O5 klātbūtnē. [Symons et al. J Chem Soc, Faraday Trans 1 76 2251 1908.] Tas arī pārkristalizējas no CH2Cl2/dietilētera un tiek žāvēts vakuumeksikatorā virs P2O5. [Blau & Espenson J Am Chem Soc 108 1962 1986, Beilstein 4 IV 657.] |
| Atsauces | [1] Banik B, et al. Tetrabutilamonija bromīda (TBAB) katalizētā bioaktīvo heterociklu sintēze. Molekulas, 2020; 25: 5918. |
| Tetrabutilamonija bromīda sagatavošanas produkti un izejvielas |
| Sagatavošanas produkti | 1-BENZOTHIOPHENE-5-CARBOXYLIC ACID-->Albendazole-->Piperonyl aldehyde-->3-AMINOBIPHENYL-->5-Bromoindazole-->ETHYL 4-ETHOXYPHENYLACETATE-->H-GLY-AMC HBR-->1-Phenylcyclopentanecarboxylic acid-->3-PHENYLBENZYLAMINE-->4-PYRIDIN-2-YLISOXAZOL-5-AMINE-->cintofen-->FENOTHIOCARB-->(R)-(-)-2,2-Dimethyl-1,3-dioxolane-4-methanol-->Isocarbophos-->Venlafaxine hydrochloride-->1-BENZOTHIOPHENE-5-CARBONITRILE-->N-(4-THIOPHEN-2-YL-PHENYL)-ACETAMIDE-->Thianaphthene-2-carboxylic acid-->Myclobutanil-->alpha-butyl-alpha-phenyl-1H-imidazole-1-propiononitrile-->5-Bromobenzo[c]thiophene-->Olaquindox-->Sisthsne-->2-[2-(DIPHENYLPHOSPHINO)ETHYL]PYRIDINE-->Glyceryl monostearate-->1-(3-Aminopropyl)piperidine-->Phenyl vinyl sulfone-->6-Bromopurine-->Methyl 3,4,5-trimethoxybenzoate-->CYCLANILIDE-->2-(4-ETHOXYPHENYL)-2-METHYL PROPIONITRILE-->Levetiracetam-->4-Bromo-7-azaindole-->DIOCTYL ETHER-->1,1-Cyclopropanedicarboxylic acid dimethyl ester-->2 -phenyl-Hexanenitrile-->Zeolite-->Tetrabutylammonium hexafluorophosphate-->4-(tert-Butyl)benzyl mercaptan-->Tetrabutilamonija borhidrīds |
Populāri tagi: tetrabutilamonija bromīds, Ķīnas tetrabutilamonija bromīda ražotāji, piegādātāji, rūpnīca
Jums varētu patikt arī
Nosūtīt pieprasījumu







