
Produkta ievads
| Hipofosforskābe Pamatinformācija |
| Ķīmiskās īpašības Izmantojumi Toksicitāte BĪSTAMĪBAS IDENTIFIKĀCIJA Sagatavošanas metode Ražošanas metode |
| Produkta nosaukums: | Hipofosforskābe |
| Sinonīmi: | HIPOFOSFORSKĀBE, 30% (W/V) šķīdums; HIPOFOSFORSKĀBE, 50% (W/V) SOLUTION; Hipofosforskābe: (Fosfīnskābe); Hipofosforskābe, 50% w/w aq. Šķīdums |
| CAS: | 6303-21-5 |
| MF: | HO2P |
| MW: | 63.980501 |
| EINECS: | 228-601-5 |
| Produktu kategorijas: | HPA;Neorganiskās vielas;6303-21-5 |
| Mol fails: | 6303-21-5.mol |
 |
|
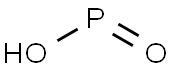
| Hipofosforskābes ķīmiskās īpašības |
| Kušanas punkts | -25 grāds |
| Vārīšanās temperatūra | 108 grādi (759,8513 mmHg) |
| blīvums | 1,206 g/ml 20 grādos (lit.) |
| tvaika spiediens | <17 mmHg ( 20 °C) |
| uzglabāšanas temp. | nekādu ierobežojumu. |
| šķīdība | ļoti labi šķīst H2O, etanolā, etilēterī |
| pka | pK1 1.1. |
| formā | higroskopiski kristāli vai bezkrāsains eļļains šķidrums |
| krāsa | Bezkrāsains |
| Šķīdība ūdenī | ŠĶĪSTĪGS |
| Merck | 13,4894 |
| Stabilitāte: | Stabils. Nesaderīgs ar spēcīgām bāzēm. Spēcīgi reaģē ar oksidētājiem, stiprām bāzēm, dzīvsudraba (II) nitrātu un dzīvsudraba (II) oksīdu. Nesildīt virs 100 C. |
| InChIKey | GQZXNSPRSGFJLY-UHFFFAOYSA-N |
| CAS datu bāzes atsauce | 6303-21-5(CAS datu bāzes atsauce) |
| NIST ķīmijas atsauce | Hipofosforskābe (6303-21-5) |
| EPA vielu reģistra sistēma | Fosfīnskābe (6303-21-5) |
| Drošības informācija |
| Bīstamības kodi | C |
| Riska paziņojumi | 34 |
| Drošības paziņojumi | 26-36/37/39-45 |
| RIDADR | ANO 3264 8/PG 3 |
| WGK Vācija | 1 |
| RTECS | SZ6400000 |
| TSCA | Jā |
| Bīstamības klase | 8 |
| Iepakojuma grupa | II |
| HS kods | 28111990 |
| Dati par bīstamām vielām | 6303-21-5(Dati par bīstamām vielām) |
| MSDS informācija |
| Pakalpojumu sniedzējs | Valoda |
|---|---|
| Fosfīnskābe | angļu valoda |
| SigmaAldrihs | angļu valoda |
| ACROS | angļu valoda |
| ALFA | angļu valoda |
| Hipofosforskābes lietošana un sintēze |
| Kontūra | Hipofosforskābe ir pazīstama arī kā "hipofosfīts". Tā ir bezkrāsaina eļļa vai šķīstošs kristāls, tas ir svarīgs smalks ķīmisks produkts. Galvenais lietojums ir kā reducētājs bezelektroniskā apšuvumam, fosfors novērš sveķu krāsas maiņu, to var izmantot arī esterifikācijas reakcijas katalizatorā, aukstumaģentā, jo īpaši augstas tīrības pakāpes nātrija hipofosfīta ražošanai. Ir vairākas sagatavošanas metodes, parastā rūpnieciskā ražošanas metode ir jonu apmaiņas sveķu metode un elektrodialīzes metode. Hipofosforskābes ķīmiskās īpašības, lietojumus, toksicitāti un ražošanas metodes ir rediģējis andy no Chemicalbook. (2016-12-04) |
| Ķīmiskās īpašības | Tie ir atšķaidoši kristāli vai bezkrāsaina eļļa. Kušanas temperatūra: 26,5 grādi. Relatīvais blīvums (īpatnējais svars): 1,439 (ciets, 19 grādi). Tas šķīst ūdenī, etanolā un ēterī, un to var sajaukt jebkurā proporcijā ar ūdeni, etanolu, acetonu. Gaisā tas viegli izšķīst līdz sīrupveida šķidrumam, un ūdens šķīdums ir skābs. Hipofosforskābe ir vienbāziska skābe, ūdens šķīdumā, Hipofosforskābe ir stipra skābe, Ka=10-2 (25 grādi); tas ir relatīvi stabils istabas temperatūrā; disproporcijas reakcija var noritēt pie 130 grādiem, sadaloties fosfīnā un fosforskābē: 2H3PO2=H3PO4+PH3 Tam ir spēcīga reducēšanās, smago metālu sāls šķīdumu var atjaunot tādos metālos kā Cu2 +, Hg2 +, Ag +, piemēram: 4Ag+H3PO2+2H2)=4Ag+H3PO4+4H+ Tas ir vājš oksidētājs, to var reducēt par fosfīnu, fosfīnu, saskaroties ar spēcīgu reducētāju. |
| Lietojumi | 1. Hipofosforskābi izmanto kā reducētāju bezelektropārklāšanai; 2. To var izmantot, lai novērstu fosforskābes sveķu krāsas maiņu; 3. To izmanto kā esterifikācijas katalizatoru, aukstumaģentu; 4. To izmanto hipofosfīta ražošanai, nātrija sāļus, mangāna sāļus, dzelzs sāļus parasti izmanto kā barojošas vielas; 5. Hipofosforskābi izmanto medicīnā un kā reducētāju, arsēna, telūra noteikšanai un tantala, niobija un citu reaģentu atdalīšanai. 6. Tas ir spēcīgs reducētājs, to var izmantot nātrija hipofosfīta, kalcija fosfāta un citu hipofosfītu pagatavošanai. 7. To var izmantot apšuvuma vannai. Farmaceitiskie izstrādājumi. reducētājs. vispārīgie reaģenti. 8. Tas ir spēcīgs reducētājs, to var izmantot nātrija hipofosfīta, kalcija fosfāta un citu hipofosfītu ražošanā. 9. Šis produkts tiek plaši izmantots kā reducētājs, Ag, Cu, Ni, Hg un citi metāli tiek reducēti līdz atbilstošajam metālam, As, Nb, Ta un citu reaģentu pārbaudei, to var izmantot Na pagatavošanai. , K, Ca, Mn, Fe un cita veida hipofosfīts. |
| Toksiskums | Tas ir nedegošs. Bet, saskaroties ar cauruma H aģentu, tas var izraisīt ugunsgrēku. Saskaroties ar oksidētāju, var notikt spēcīga reakcija un degšana. Kad tas tiek uzkarsēts līdz augstam līmenim, tas var sadalīties ļoti toksiskā fosfīna gāzē vai pat eksplodēt. Tas ir kodīgs. Hipofosforskābi bieži pievieno bezalkoholiskajiem dzērieniem un tāpēc, ka tā netiek absorbēta. Tātad risks ir mazs, bet īpaši spēcīgs hipofosfīts ievainots kuņģa-zarnu traktā. Nejauši tas izšļakstās acīs vai saskaras ar ādu, mazgāšanai tiek izmantots daudz ūdens. Ražošanas operatoriem jāvalkā aizsargapģērbs un cits aizsargtērps. Ražošanas iekārtai jābūt noslēgtai, darbnīcai jābūt labi vēdinātai. |
| BĪSTAMĪBAS APZINĀŠANA | Bīstamības paziņojums: Izraisa smagus ādas apdegumus un acu bojājumus. Izraisa nopietnus acu bojājumus Piesardzības paziņojumi: Neieelpot putekļus/dūmus/gāzi/miglu/tvaikus/smidzinājumu. Pēc apstrādes rūpīgi nomazgājiet. Valkājiet aizsargcimdus un acu/sejas aizsargus. NORĪŠANAS GADĪJUMĀ: izskalot muti. NEIZRAISĪT vemšanu. SASKARĒ AR ĀDU (vai matiem): Nekavējoties novilkt/novilkt visu piesārņoto apģērbu. Noskalojiet ādu ar ūdeni/dušā. SASKARĒ ACĪS: uzmanīgi skalot ar ūdeni vairākas minūtes. Izņemiet kontaktlēcas, ja klāt un viegli izdarāms. Turpiniet skalošanu. IEELPOŠANAS GADĪJUMĀ: izvest cietušo svaigā gaisā un turēt miera stāvoklī, lai būtu ērti elpot. Nekavējoties sazinieties ar SAINDĒŠANĀS CENTRU vai ārstu. Glabājiet aizslēgtu. Izmest šo materiālu un tā tvertni bīstamo vai speciālo atkritumu savākšanas punktā. |
| Sagatavošanas metode | 1. Fosfora un bārija hidroksīda šķīdumu karsē, var veidoties bārija sāls Ba (H2PO2) 2 • 2H2O, sērskābi pievieno hipofosforskābes bārija šķīdumam, Ba2+ var izgulsnēties: Ba(H2PO2)2+H2SO4=BaSO4+2H3PO2 Hipofosforskābi var iegūt, iztvaicējot pazeminātā spiedienā un kristalizējot zemā temperatūrā. Tā kā šajā procesā bārija sāls šķīdība ir maza, tāpēc iegūtās hipofosforskābes koncentrācija nav augsta, rūpnieciskais produkts ir jāattīra ar pārkristalizāciju. 2. bārija oksīdu (vai kaļķi) un baltā fosfora šķīdumu karsē kopā, veidojot sekundāro bārija fosfātu (vai kalciju), un pēc tam reaģē ar sērskābi, to filtrē, koncentrē, lai iegūtu produktu vai nātrija hipofosfīta šķīdumā veidojas H- tipa jonu apmaiņas sveķi var iegūt produktu. Šai metodei nepieciešams liels daudzums sveķu, un sveķu reģenerācijas un mazgāšanas posms ir apgrūtinošs, parasti tas maksā vairāk nekā 7 USD par mārciņu, tā ir piemērota tikai nelielu sēriju ražošanai un nav piemērota liela mēroga rūpnieciskiem lietojumiem. 3. Hipofosforskābi sagatavo ar elektrodialīzes metodi, kur elektrodialīzes šūna sadalās trīs daļās, tās ir anoda kamera, izejmateriāla kamera un katoda kamera, starpproduktu atdala ar anjonu membrānu un katjonu membrānu, starp divām membrānām ievieto nātrija hipofosfīta šķīdumu. (koncentrācija 100g/l~500g/l), anoda kamera ir atšķaidīts hipofosforskābes šķīdums 5g/L, anoda kamera ir atšķaidīts nātrija hidroksīda šķīdums (5g/L), starp poliem tiek izvadīts DC (3V~36V), anods izdala skābekli un rada sekundāro hipofosforskābes produktu; katods izstaro ūdeņradi un ģenerē sekundāro nātrija hidroksīda produktu, reakcijas laiks ir 3–21 h. Anoda kameras un katoda kameras reakcijas ir šādas: anoda kamera: H2O==H++OH- 2OH-==O2+2H2O+4e H++H2PO2-==H3PO2 katoda kamera: H2O==H++OH- 2H++2e==H2 Na++OH-==NaOH Elektrodialīzes sagatavošanas metode Hipofosforskābe ir vienkārša un iekārtu investīcijas ir nelielas, piemērota masveida ražošanai. 4. Sākot no rūpnieciskās kvalitātes nātrija hipofosfīta, Cl-, SO42-anjoni, kas ietekmē hipofosforskābes kvalitātes rādītājus, tiek noņemti ar nokrišņiem, smago metālu joni tiek izņemti no šķīduma, veidojot sulfīdu, un pēc tam izmantojot stipru skābi. katjonu apmaiņas sveķus, lai iegūtu nātrija sekundāro fosfātu, var iegūt augstas tīrības pakāpes produktu. Process var ražot augstas kvalitātes sekundāro fosfātu, tehniski ir iespējams, process ir vienkāršs, viegli lietojams, laba produkta kvalitāte, tas var apmierināt elektronikas rūpniecības, aizsardzības rūpniecības un citu augsto tehnoloģiju jomu vajadzības. 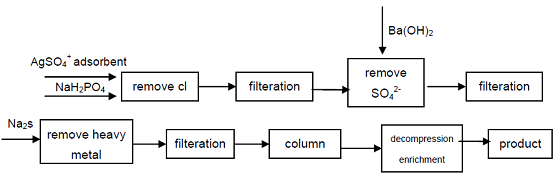 1. attēls Hipofosforskābes ražošanas process no rūpnieciskā nātrija hipofosfīta. 5. Jonu apmaiņas sveķu metode: apmēram 70 g katjonu apmaiņas sveķu, kas samitrināti ar ūdeni, iepilda stikla mēģenē ar 5 mol/L sālsskābi, kas cirkulē apmēram 15 minūtes, pēc rūpīgas mazgāšanas ar ūdeni, augstas tīrības pakāpes nātrija hipofosfīta ūdens šķīdumu (15 g/ Caur to izplūst 60 ml H2O), sveķu kolonnu vispirms mazgā ar 50 ml, pēc tam ar 25 rnl destilēta ūdens. Izplūdušo skābi un mazgāšanu apvieno, to koncentrē, iztvaicējot ūdens vannā. Koncentrēto skābi ievieto augstā vakuumā ar P205 žāvētāju dehidratācijai, dzesēšanai un kristalizācijai, filtrēšanai, pārkristalizācijai, lai iegūtu hipofosforskābes produktu. |
| Ražošanas metode | Jonu apmaiņas sveķu metode: ielieciet apmēram 70 g ūdenī šķīstošu katjonu apmaiņas sveķu, lai iepildītu stikla mēģenē. Apmēram 15 minūtes cirkulē ar 5 mol/l sālsskābi un pietiekami mazgā ar ūdeni. Caur sveķu kolonnu izplūst nātrija hipofosfīta ūdens šķīdums ar augstu ūdens saturu (15 g/60 ml H2O), pēc tam to vispirms mazgā ar 50 ml ūdens un pēc tam skalo ar 25 ml destilēta ūdens. Izplūdušā skābe un mazgāšanas līdzekļi tika apvienoti un koncentrēti, iztvaicējot ūdens vannā. Koncentrētā skābe tiek nosūtīta uz augsta vakuuma P205 žāvētāju dehidratācijai, kam seko dzesēšanas kristalizācija, filtrēšana un pārkristalizācija, lai iegūtu gatavo hipofosforskābes produktu. |
| Apraksts | Hipofosforskābe ir spēcīgs reducētājs ar H3PO2 molekulāro formulu. Neorganiskie ķīmiķi brīvo skābi dēvē ar šo nosaukumu, lai gan tās IUPAC nosaukums ir dihidrohidroksidoksidofosfors jeb pieņemamais fosfīnskābes nosaukums. Tas ir bezkrāsains savienojums ar zemu kušanas temperatūru, kas šķīst ūdenī, dioksānā un spirtos. Hipofosforskābes formula parasti ir rakstīta H3PO2, bet aprakstošāks ir HOP(O)H2, kas izceļ tās monoprotisko raksturu. Sāļus, kas iegūti no šīs skābes, sauc par fosfinātiem (hipofosfītiem). |
| Apraksts | Šai skābei ir vispārīgā formula H4P2O6, un tā atšķiras no pārējām oksifosforskābēm. Tam ir daudz īpatnību. Tas veidojas kopā ar fosforu un fosforskābēm, kad fosfors tiek oksidēts mitrā gaisā. Ja baltais fosfors tiek pakļauts gaisam un šķidrumam, kas veidojas, tiek pievienots nātrija acetāts, atdalās nedaudz nešķīstošs nātrija hipofosfāts, Na2H2P2O6·6H2O. Tomēr nātrija hipofosfāta monohidrāts ir ļoti labi šķīstošs un šķidrs, ja ir -98,7 g/100 ml. |
| Ķīmiskās īpašības | bezkrāsains šķidrums |
| Fizikālās īpašības | Bezkrāsaini šķīstoši kristāli vai eļļains šķidrums; skāba smaka; blīvums 1,493 g/cm3;kūst pie 26,5 grādiem ; vārās 130 grādos; ļoti labi šķīst ūdenī, spirtā un ēterī; 50% ūdens šķīduma blīvums ir 1,13 g/ml. |
| Lietojumi | Hipofosforskābi galvenokārt izmanto bezelektroniskā niķeļa pārklāšanai. Tas ir iesaistīts arenēdiazonija sāļu reducēšanā. Tas darbojas kā piedeva Fišera esterifikācijas reakcijās. Tas kalpo arī kā neitralizators, antioksidants, katalizators polimerizācijā un polikondensācijā, kā arī mitrinātājs. Turklāt to izmanto farmaceitisko preparātu pagatavošanai, polimēru krāsas maiņai, ūdens attīrīšanai un dārgmetālu vai krāsaino metālu ieguvei. Papildus tam to izmanto kā balinātājus plastmasām, sintētiskajām šķiedrām, atkrāsojošo līdzekli un krāsas stabilizēšanai ķīmisko vielu un vairāku plastmasu ražošanā. |
| Sagatavošana | Hipofosforskābi var pagatavot ar dažādām metodēm: 1. Baltā fosfora vārīšana ar kalcija hidroksīdu: P4+ 4Ca(OH)2 + 8H2O → 4Ca(H2PO2)2 + 4H2 Kalcija sāls šķīst ūdenī. Apstrādājot ar sērskābi, tiek iegūta hipofosforskābe: (H2PO2)2Ca + H2SO4 → 2H3PO2+ CaSO4 Produkta maisījumu filtrē, lai atdalītu nešķīstošo CaSO4. Hipofosforskābes ūdens šķīdumu koncentrē pazeminātā spiedienā.Kalcija hidroksīda vietā var izmantot koncentrētu barīta ūdeni.2. Apstrādājot nātrija hipofosfītu, NaH2PO2 ar jonu apmaiņas sveķiem. Nātrija sāli var iegūt, vārot balto fosforu ar nātrija hidroksīda šķīdumu, reakcija ir līdzīga iepriekš (1) aprakstītajai reakcijai. PH3 + 2I2 + 2H2O → H3PO2+ 4SVEIKAS! Iepriekš minēto metodi var uzskatīt par drošāku par balto fosfora karsēšanu ar sārmu. Hipofosforskābe jāuzglabā zem 50 grādiem. To pārdod komerciāli kā ūdens šķīdumu dažādās koncentrācijās. |
| Ražošanas metodes | Hipofosforskābe veidojas, reaģējot bārija hipofosfītam ar sērskābi un filtrējot bārija sulfātu. Iztvaicējot šķīdumu vakuumā pie 80 grādiem un pēc tam atdzesējot līdz 0 grādiem, hipofosforskābe kristalizējas. |
| Definīcija | ChEBI: Fosfora oksoskābe, kas sastāv no viena piecvērtīga fosfora, kas kovalenti saistīts ar vienu saiti ar diviem ūdeņraža atomiem un hidroksigrupu un caur dubultsaiti ar skābekli. Fosfīnskābju klases vecākais. |
| Definīcija | Balta kristāliska cieta viela. Tā ir vienbāziska skābe, kas veido anjonu H2PO2- ūdenī. Nātrija sāli un līdz ar to arī skābi var pagatavot, karsējot dzelteno fosforu ar nātrija hidroksīda šķīdumu. Brīvā skābe un tās sāļi ir spēcīgi reducējoši līdzekļi. |
| Reakcijas | Hipofosforskābe visās proporcijās sajaucas ar ūdeni, un komerciālais stiprums ir 30% H3PO2. Hipofosfītus izmanto medicīnā. Hipofosforskābe ir spēcīgs reducētājs, piemēram, ar vara sulfātu veidojas vara hidrīds Cu2H2, brūnas nogulsnes, kas izdala ūdeņraža gāzi un, sasilstot, atstāj varu; ar sudraba nitrātu iegūst smalki sadalītu sudrabu; ar sērskābi iegūst sēru un nedaudz sērūdeņraža; ar sērskābi iegūst sērskābi, kas reaģē kā iepriekš; uzreiz ar permanganātu veido mangāna gaisotni. |
| Vispārīgs apraksts | Hipofosforskābe parādās kā bezkrāsains eļļains šķidrums vai šķīstoši kristāli ar skābu smaržu. Blīvums 1,439 g / cm3. Kušanas temperatūra 26,5 grādi. Tvaiku ieelpošana kairina vai sadedzina elpceļus. Šķidrums un tvaiki var kairināt vai apdedzināt acis un ādu. |
| Gaisa un ūdens reakcijas | Atšķaidošs. Ūdenī šķīstošs. |
| Reaktivitātes profils | HIPOFOSFORSKĀBE karsējot sadalās par fosforskābi un spontāni uzliesmojošu fosfīnu. Tiek oksidēts ar sērskābi, izdalot sēra dioksīdu un sēru. Sprādzienbīstami reaģē ar dzīvsudraba(II) oksīdu [Mellor, 1940, Vol. 4, 778]. Spēcīgi reaģē ar dzīvsudraba(II) nitrātu [Mellor, 1940, Vol. 4, 993]. Eksotermiskās reakcijās neitralizē bāzes. |
| Apdraudējums | Ugunsgrēka un sprādziena risks saskarē ar oksidētājiem. |
| Veselības apdraudējums | TOKSISKI; materiāla ieelpošana, norīšana vai saskare ar ādu var izraisīt smagus savainojumus vai nāvi. Saskare ar izkausētu vielu var izraisīt smagus ādas un acu apdegumus. Izvairieties no jebkādas saskares ar ādu. Saskares vai ieelpošanas sekas var būt aizkavētas. Uguns var radīt kairinošas, kodīgas un/vai toksiskas gāzes. Ugunsdzēsības vai atšķaidīšanas ūdens notece var būt kodīga un/vai toksiska un izraisīt piesārņojumu. |
| Ugunsbīstamība | Nedegoša, viela pati par sevi nedeg, bet karsējot var sadalīties, veidojot kodīgus un/vai toksiskus izgarojumus. Daži no tiem ir oksidētāji un var aizdedzināt uzliesmojošas vielas (koksni, papīru, eļļu, apģērbu utt.). Saskaroties ar metāliem, var izdalīties uzliesmojoša ūdeņraža gāze. Karsējot tvertnes var eksplodēt. |
| Attīrīšanas metodes | Fosforskābe ir izplatīts komerciālās 50% hipofosforskābes piesārņotājs. Dženkinss un Džonss [J Am Chem Soc 74 1353 1952] attīrīja šo materiālu, iztvaicējot apmēram 600 ml 1 l kolbā 40 ° temperatūrā, zem samazināta spiediena (N2) līdz apmēram 300 ml tilpumam. Pēc šķīduma atdzesēšanas to pārnesa uz platmutes Erlenmeijera kolbu, kas tika aizbāzta un atstāta sausā ledus/acetona vannā vairākas stundas, lai sasalst (ja nepieciešams, skrāpējot sienu). Kad kolba tika atstāta apmēram 5o temperatūrā uz 12 stundām, apmēram 30-40% no tās sašķidrināja un atkal tika filtrēta. Šo procesu atkārtoja, pēc tam cieto vielu uzglabāja virs Mg(ClO4)2 vakuumeksikatorā aukstumā. Turpmākās kristalizācijas no n-butanola, izšķīdinot to istabas temperatūrā un pēc tam atdzesējot ledus-sāls vannā pie -20o, to neattīrīja. Brīvā skābe veido šķīstošus kristālus m 26,5o un šķīst H2O un EtOH. NaH2PO2 sāli var attīrīt, izmantojot anjonu apmaiņas sveķus [Klement Z Anorg Allgem Chem 260 267 1949.] |
| Hipofosforskābes preparāti un izejvielas |
| Izejvielas | AMBERLITE(R) IRC-50 |
| Sagatavošanas produkti | XANTHURENIC ACID-->3,5-diisopropylphenol-->cmtirust agent T-708-->Sodium hypophosphite-->TRIS(2,2'-BIPYRIDYL)RUTHENIUM(II) CHLORIDE HEXAHYDRATE-->4-IODOPYRIDINE-2-CARBOXYLIC ACID-->2,3,5,6-Tetrafluorophenol-->Benzothiazole, 4-methyl- (7CI,8CI,9CI)-->BEHENIC ACID METHYL ESTER-->Fosforskābe |
Populāri tagi: hipofosforskābe, Ķīnas hipofosforskābes ražotāji, piegādātāji, rūpnīca
Pāri: Kālija bromāts
Nākamo: Fluorborskābe
Jums varētu patikt arī
Nosūtīt pieprasījumu



