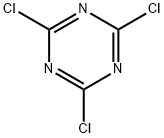
| Kontūra |
Cianūrhlorīds, balti kristāli ar spēcīgu kairinošu hlora smaržu, ir kodīgs ādai, tam piemīt acu kairinājuma un asarošanas īpašības. Kušanas temperatūra 145 grādi, viršanas temperatūra 190 grādi, UVλmax241 nm (etanols). Šķīst etanolā, etilēterī, hloroformā, etiķskābē un akrilnitrilā, nešķīst aukstā ūdenī. Cianūrhlorīda un ūdens reakcijas atdzesēšana notiek lēni, karsējot ātri hidrolizējas par cianurskābi (C3H3O3N3) un sālsskābi, produkts salīdzinoši šķīst ūdenī, tāpēc var izmantot atdalīšanas ekstrakcijas metodi. Tas reaģē ar koncentrētu slāpekļskābi un koncentrētu sērskābi istabas temperatūrā, lai daļēji pārveidotu ciānskābi, un tas reaģē ar nātrija alkoksīdu, veidojot ciānskābes triesteri, un tas var reaģēt arī ar amonjaku, amīniem, fenoliem un tā tālāk.
Pēdējos gados Ķīnā ir vērojams straujš cianūrhlorīda patēriņa pieaugums, no 1998. gada līdz 2{10}}04. gada vidējais acīmredzamā patēriņa pieauguma temps bija aptuveni 32,2%, 2005. gadā pieprasījums pēc cianūrhlorīda sasniedza 50,{{ 6}} tonnas, saskaņā ar prognozēm, no 2007. līdz 2012. gadam cianurskābes hlorīds turpinās strauju pieaugumu vidēji 6,0% apmērā, tirgus ir ļoti daudzsološs. Tā kā turpmākie cianūrhlorīda produkti ir milzīgi, tirgus pieprasījums ir liels, valsts pētniecības iestādes un saistītie uzņēmumi ir turpinājuši izstrādāt pakārtotos produktus un atvērt cianurhlorīda lietojumus. Tāpēc parādās jauns produkts ar cianurskābes hlorīda atvasinājumiem, un tirgus pieprasījums tiks vēl vairāk paplašināts.
Saistītās cianūrhlorīda ķīmiskās reakcijas, kas ietver:
Pēc 2-amino-4-nitrofenola diazotēšanas un H skābes savienošanas un hroma, kobalta kompleksa pēcapstrādes tas vispirms tiek kondensēts ar cianurhlorīdu, pēc tam pēc kondensācijas ar amonjaku, lai iegūtu reaktīvo melno K-BR. To galvenokārt izmanto kokvilnas, poliestera / kokvilnas apdrukai.
Izmantojot ciānurskābes hlorīdu kā izejvielu, trihloretilēna šķīdumā 20-30 grādu temperatūrā amīna reakcijā tiek iegūts 2,4-dihlor-6-etil-1,3,5-triazīns. veidojas, un tad tas reaģē ar amonjaku, veidojot 2-amino-4-hloro-6-etilaminotriazīnu, un pēc tam tas reaģē ar 2-hlor-2-metilpropionitrilu, kas var radīt selektīvus herbicīdus cianazīnu viengadīgo vai daudzgadīgo šauru lapu vai platlapju nezāļu kontrolei kukurūzas laukos. |
| Ķīmiskās īpašības |
Kristāli Ar asu smaku. Šķīst hloroformā, tetrahlorogleklī, etanolā, karstā ēterī, acetonā, dioksānā, nedaudz šķīst ūdenī. |
| Lietojumi |
cianūrhlorīds ir svarīgs smalks ķīmisks produkts ar plašu lietojumu klāstu, tas ir starpprodukts pesticīdu rūpniecībā un reaktīvo krāsvielu izejmateriālu ražošanā, to var izmantot kā visa veida organiskās rūpnieciskās ražošanas piedevas, piemēram, fluorescējošos balinātājus, tekstilizstrādājumu saraušanās necaurlaidīgas vielas, virsmas aktīvās vielas, tas ir viens no materiāliem, ko izmanto aizsardzības sprāgstvielu un gumijas paātrinātāju ražošanā, un tas ir arī materiāls narkotiku sintēzei pesticīdu un farmācijas rūpniecībā.
Iepriekš minētā informācija ir rediģēta Tian Ye ķīmiskajā grāmatā. |
| ražošanas metode |
Cianūrhlorīda ražošanas process parasti sastāv no diviem posmiem: hlorīda cianogēna polimerizācijas un hlorīda cianogēna sagatavošanas. Ir daudz veidu, kā iegūt hlorīda ciānogēnu, piemēram, metiltiocianāta un hlora sintēze, ciānūdeņražskābe tiek izšķīdināta hloroformā un sintezēšanai tiek ievadīta hlora gāze, ciānūdeņražskābes metode, nātrija cianīda, urīnvielas, ciānūdeņražskābes tiešā hlora metode un ciānskābes hlorīds un tamlīdzīgi, pašreizējā rūpnieciskā cianūrhlorīda ražošanā parasti izmanto nātrija cianīdu un ciānūdeņražskābi kā izejvielas divos veidos. 1. Nātrija cianīda metode: izmantojot nātrija cianīdu kā izejvielu pēc hlora un cianurskābes hlorīda reakcijas, tas tiek polimerizēts, veidojot cianurskābes hlorīdu, tas tiek dzēsts, pēc tam pēc kristalizācijas tiek iegūts produkts. Materiāla patēriņš fiksēts: nātrija cianīds 1073kg/t, hlors 1700kg/t. 2. Ciānūdeņražskābes metode: izmantojot ciānūdeņražskābi kā izejvielu, hlorīda ciānogēnu iegūst, reaģējot ar hloru, un pēc tam izmanto polimerizāciju, lai iegūtu ciānskābes hlorīdu, atdzesē, kristalizē, iegūst produktu. Materiāla patēriņš fiksēts: ciānūdeņražskābe 500kg/t, hlors 1200kg/t. |
| Kategorija |
kodīgas vielas |
| Toksicitātes klasifikācija |
Vidēji toksisks |
| Akūta toksicitāte |
Iekšķīgi žurkām LD50: 485 mg/kg; Oral-Mouse LD50: 350 mg/kg |
| Kairinājuma dati |
āda-truša 500 mg/24 stundas mēreni; Acis-truša 0,05 mg/24 stundas smagas |
| Uzliesmojamības un bīstamības īpašības |
Saskaroties ar ūdeni, tas izdala toksisku hlorūdeņraža gāzi; ja tas ir termisks, tas sadala toksisko hlorūdeņraža gāzi |
| Uzglabāšanas īpašības |
Ventilēta, zemas temperatūras, sausa noliktava. Uzglabā atsevišķi no oksidētājiem un sārmiem. |
| Ugunsdzēšanas līdzeklis |
oglekļa dioksīds, sausais pulveris, smilšaina augsne |
| Ķīmiskās īpašības |
Balts pulveris |
| Lietojumi |
Cianurhlorīds ir starpprodukts agroķīmisko vielu (triazīna herbicīdu), krāsvielu, optisko balinātāju, miecvielu, reaktīvo krāsvielu, UV absorbcijas līdzekļu, mīkstinātāju un farmaceitisko līdzekļu, kā arī plastmasas bloku veidotāju ražošanā. Produkta datu lapa |
| Lietojumi |
Cianurhlorīds ir starpprodukts agroķīmisko vielu, krāsvielu, optisko balinātāju, miecvielu, mīkstinātāju un farmaceitisko līdzekļu, kā arī plastmasas bloku veidotāju ražošanā. |
| Lietojumi |
Reaģents spirtu pārvēršanai hlorīdos un mikroorganismu un fermentu imobilizācijai.1 |
| Lietojumi |
Cianūrhlorīds tiek plaši izmantots triazīna klases pesticīdu un herbicīdu pagatavošanā. Cianūrhlorīds tiek izmantots arī kā krāsvielu un šķērssaistīšanas līdzekļu prekursors, jo hlora atomi reaģē uz nukleofīlo aizvietošanas reakcijām. Cianūrhlorīda atvasinājumiem ir plašs darbību spektrs kā antibakteriāliem un pretvēža līdzekļiem. |
| Lietojumi |
Starpprodukts aktīvo krāsvielu, lauksaimniecības produktu un ārstniecisko vielu sintēzē. Reaģents organiskajā sintēzē. Savienojošs līdzeklis nukleīnskābēm un olbaltumvielām; Ar cianūrhlorīdu aktivētu papīru izmanto kapilāros un elektroblotēšanas lietojumos, punktu testos un hibridizācijas protokolos. |
| Definīcija |
ChEBI: hlor-1,3,5-triazīns, kurā triazīna gredzens katrā oglekļa atomā ir aizstāts ar hloru. To galvenokārt izmanto triazīna klases pesticīdu pagatavošanā. |
| Ražošanas metodes |
Cianūrhlorīdu iegūst, trimerizējot ciānhlorīdu organiskos šķīdinātājos skābu katalizatoru klātbūtnē, un to veic gāzveida fāzē 200–500 C temperatūrā. Cianūrhlorīdu izmanto kā ķīmisko starpproduktu. Tas ir herbicīda atrazīna prekursors. |
| Vispārīgs apraksts |
Bezkrāsaina kristāliska cieta viela ar asu smaržu. Kušanas temperatūra 146 grādi. Blīvums 1,32 g / cm3. Ļoti nedaudz šķīst ūdenī. Toksisks, norijot un ieelpojot tvaikus. Kairina ādu un acis. Izmanto krāsvielu izgatavošanai. |
| Gaisa un ūdens reakcijas |
Eksotermiski reaģē ar ūdeni, īpaši, ja tas tiek katalizēts vai karsēts, veidojot sālsskābes izgarojumus. Ļoti nedaudz šķīst ūdenī. |
| Reaktivitātes profils |
Cianūrhlorīds ātri un eksotermiski reaģē ar ūdeni, veidojot hlorūdeņradi. Maisījums ar ūdeni rūpnieciskajā reaktorā ar dzesēšanu izslēdza spiedienu, kas izpūta blīves un piepildīja ēku ar viegli uzliesmojošiem tvaikiem. Kad tvaiki tika aizdedzināti, notika sprādziens [MCA Case History 1869(1972)]. Bēgšanas reakcijas ir notikušas ar acetonu/ūdeni; metanols/ūdens, etoksietanols/ūdens, alilspirts/nātrija hidroksīds/ūdens, 2-butanons/nātrija hidroksīds/ūdens un metanols/nātrija bikarbonāts [Zudums Iepriekš. Bull., 1979, (25), 21]. Reaģē ar metanolu, veidojot gāzveida metilhlorīdu. Ātri reaģē ar bikarbonātiem, veidojot gāzveida oglekļa dioksīdu. Spēcīgi reaģē ar dimetilformamīdu (DMF), veidojot oglekļa dioksīdu pēc maldinoša indukcijas perioda [BCISC Quart. Drošības kopsavilkums, 1960, 35, 24]. Var reaģēt ar reducētājiem, radot siltumu un produktus, kas var būt gāzveida (izraisot spiedienu slēgtās tvertnēs). Produkti paši var būt spējīgi veikt turpmākas reakcijas (piemēram, sadegšanu gaisā). |
| Veselības apdraudējums |
TOKSISKI; ieelpošana, norīšana vai saskare (āda, acis) ar tvaikiem, putekļiem vai vielu var izraisīt smagus savainojumus, apdegumus vai nāvi. Reakcijā ar ūdeni vai mitru gaisu izdalīsies toksiskas, kodīgas vai viegli uzliesmojošas gāzes. Reakcija ar ūdeni var radīt daudz siltuma, kas palielinās izgarojumu koncentrāciju gaisā. Uguns izdalīs kairinošas, kodīgas un/vai toksiskas gāzes. Ugunsgrēka kontroles vai atšķaidīšanas ūdens notece var būt kodīga un/vai toksiska un izraisīt piesārņojumu. |
| Ugunsbīstamība |
Nedegoša, viela pati nedeg, bet karsējot var sadalīties, veidojot kodīgus un/vai toksiskus izgarojumus. Tvaiki var uzkrāties slēgtās vietās (pagrabā, tvertnēs, tvertnēs/cisternās utt.). Viela reaģēs ar ūdeni (daži spēcīgi), izdalot kodīgas un/vai toksiskas gāzes un noteci. Saskaroties ar metāliem, var izdalīties uzliesmojoša ūdeņraža gāze. Karsējot vai piesārņojot ar ūdeni, tvertnes var eksplodēt. |
| Uzliesmojamība un sprādzienbīstamība |
Nedegošs |
| Drošības profils |
Saindē, norijot, ieelpojot un intravenozi. Apšaubāms kancerogēns ar eksperimentāliem audzēju izraisošiem datiem. Eksperimentālā reproduktīvā ietekme. Kodīgs līdzeklis. Ādas un smags acu kairinātājs. Alergēns. Ir ziņots, ka tas izraisa gļotādu kairinājumu un sirds ritma traucējumus cilvēkiem. Spēcīga reakcija ar ūdeni - (virs 30 grādiem), acetons + ūdens, metanols, metanols + nātrija hidrogēnkarbonāts, 2- etoksietanols, dimetilformamīds, 3- butanons + nātrija hidroksīds + ūdens, alilspirts + nātrija hidroksīds + ūdens (pie 28 grādiem). Sildot līdz sadalīšanai, tas izdala toksiskus Cland NOx dūmus. Skatīt arī HLORĪDI. |
| Attīrīšanas metodes |
TCT kristalizējas no CCl4 vai petētera (b 90-100o) un tiek žāvēts vakuumā. Tas ir arī divreiz pārkristalizēts no bezūdens *benzola tieši pirms lietošanas [Abuchowski et al. J Biol Chem 252 3582 1977]. [Beilšteina 26 III/IV 66.] |