
Produkta ievads
| Kalcija fluorīds Pamatinformācija |
| Ķīmiskās īpašības kristāla struktūra Izmanto Ražošanas metodi |
| Produkta nosaukums: | Kalcija fluorīds |
| Sinonīmi: | Kalcija fluorīds; Kalcija fluorīds, 99,9% metālu bāzes; Kalcija fluorīds, 99,95% metālu bāzes; Bezūdens kalcija fluorīds, ampulēts argonā, 99,99% metālu mikroelementu bāzes; kalcija fluorīds Ķīnā; antiviela (ANTI-TERM)8 ražots trušiem;CAF1-līdzīgs proteīns;CALIFp |
| CAS: | 7789-75-5 |
| MF: | CaF2 |
| MW: | 78.07 |
| EINECS: | 232-188-7 |
| Produktu kategorijas: | Neorganiskās vielas; metālu halogenīds |
| Mol fails: | 7789-75-5.mol |
 |
|
| Kalcija fluorīda ķīmiskās īpašības |
| Kušanas punkts | 1402 grādi |
| Vārīšanās temperatūra | 2500 grādi (lit.) |
| blīvums | 3,18 g/ml 25 grādos (lit.) |
| refrakcijas indekss | 1.434 |
| Fp | 2500 grādi |
| uzglabāšanas temp. | -20 grāds |
| šķīdība | Nedaudz šķīst skābē; nešķīst acetonā. |
| formā | stienis |
| krāsa | balts |
| Īpatnējais smagums | 3.18 |
| Šķīdība ūdenī | 0,015 g. uz 100 g H20 istabas temperatūrā. (NEŠĪSTĪGS) |
| Jūtīgs | Higroskopisks |
| Merck | 14,1667 |
| Šķīdības produkta konstante (Ksp) | pKsp: 8,28 |
| Ekspozīcijas robežas | ACGIH: TWA 2,5 mg/m3 NIOSH: IDLH 250 mg/m3; TWA 2,5 mg/m3 |
| Dielektriskā konstante | 2,5 (vides režīms) |
| Stabilitāte: | Stabils. Kalcija fluorīds ir inerts pret organiskām ķīmiskām vielām un daudzām skābēm, tostarp HF. Tas lēnām izšķīst slāpekļskābē. |
| InChIKey | WUKWITHWXAAZEY-UHFFFAOYSA-L |
| CAS datu bāzes atsauce | 7789-75-5(CAS datu bāzes atsauce) |
| NIST ķīmijas atsauce | Kalcija fluorīds (7789-75-5) |
| EPA vielu reģistra sistēma | Kalcija difluorīds (7789-75-5) |
| Drošības informācija |
| Bīstamības kodi | Xi, Xn |
| Riska paziņojumi | 36/37/38 |
| Drošības paziņojumi | 26-37/39-36 |
| RIDADR | 3288 |
| WGK Vācija | 1 |
| RTECS | EW1760000 |
| Bīstamības piezīme | Kairinošs |
| TSCA | Jā |
| HS kods | 28261900 |
| Dati par bīstamām vielām | 7789-75-5(Dati par bīstamām vielām) |
| Toksiskums | LD50 ip pelēm: 2638,27 mg/kg (Stratmann) |
| MSDS informācija |
| Pakalpojumu sniedzējs | Valoda |
|---|---|
| Kalcija fluorīds | angļu valoda |
| SigmaAldrihs | angļu valoda |
| ACROS | angļu valoda |
| ALFA | angļu valoda |
| Kalcija fluorīda lietošana un sintēze |
| Ķīmiskās īpašības | Kalcija fluorīds ir fluoršpata vai fluorīta galvenā sastāvdaļa, ķīmiskā formula ir CaF2, tas ir bezkrāsains kubiskais kristāls vai balts pulveris. Relatīvais blīvums ir 3,18, kušanas temperatūra ir 1423 grādi, viršanas temperatūra ir aptuveni 2500 grādi. Šķīdība ūdenī ir minimāla, 100g ūdens var izšķīdināt tikai 0,0016g pie 18 grādiem, tas nešķīst acetonā, bet šķīst sālsskābes, fluorūdeņražskābes, sērskābes, slāpekļskābes un amonija sāls šķīdumā un nevar reaģēt ar atšķaidītu skābe, bet var reaģēt ar karstu koncentrētu sērskābi un radīt fluorūdeņražskābi, tā var veidot kompleksu, kad izšķīst alumīnija un dzelzs sāļu (Fe3 +) šķīdumā. Dabīgais kalcija fluorīds ir minerālu fluorīts vai fluoršpats, bieži ir pelēks, dzeltens, zaļš, purpursarkans un citas krāsas, dažreiz tas ir bezkrāsains, caurspīdīgs, spīdīgs stikls, trausls, un relatīvais blīvums ir 3,01–3,25, tam ir ievērojama fluorescences parādība. To var izmantot kā fluora avotu un materiālu fluorūdeņražskābes sistēmas, fluorīda, ražošanai; un to var izmantot arī stikla, emaljas, glazūras ražošanā. Fluorītu galvenokārt izmanto kā plūsmu metalurģijā, no ļoti tīra fluoršpata var izgatavot īpašas lēcas. Ja ūdens satur (1–1,5) × 10-6 kalcija fluorīdu, tas var novērst zobu problēmas. Turklāt to var izmantot dzelzs un tērauda kausēšanā, ķīmisko vielu, stikla, keramikas ražošanā. Tīru produktu var izmantot dehidratācijas, dehidrogenēšanas katalizatoram. Šķīstošo kalcija sāļu (kalcija karbonāta vai kalcija hidroksīda) un nātrija fluorīda vai fluorūdeņražskābes ietekmē var iegūt amonija fluorīdu, kalcija fluorīdu. |
| kristāla struktūra | Kalcija fluorīds ir jonu kristāls ar fluora anjoniem vienkāršā kubiskā blokā un kalcija katjoniem pusē no struktūras kubiskajām vietām. Var arī uzskatīt, ka kalcija joni atrodas uz "paplašināta" fcc režģa ar fluora joniem, kas izraisa to režģa atdalīšanos 0,39 nm. Šis attēlojums ir parādīts apakšējā diagrammā. Vienības šūnā ir 4 Ca2+joni un 8 F1-joni.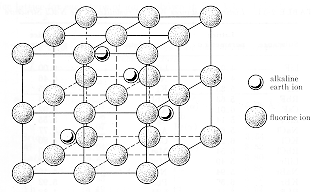 Materiāls ir caurspīdīgs redzamajā spektrālajā reģionā un parāda elektronisko optisko adsorbciju ultravioletajā starā un režģa optisko absorbciju infrasarkanajā starā. |
| Lietojumi |
Rūpniecība
Pieteikums
Loma/ieguvums
Ķīmiskā ražošana
Fluorūdeņražskābes un fluorīda ražošana
Izejviela/fluorīda avots
Fluora smalko ķīmisko vielu un sintētiskā kriolīta ražošana
Izejviela/fluorīda avots
Arhitektūras materiāls
Stikla ražošana
Fluksētājs/veicina izejvielu kušanu
Cementa ražošana
Mineralizācijas līdzeklis
Keramikas glazūras izgatavošana
Plūsmas un krāsošanas palīglīdzekļi
Metalurģija
Dzelzs un tērauda kausēšana, dzelzs sakausējumu ražošana utt.
kušanas līdzeklis/samazināt ugunsizturīgo vielu kušanas temperatūru
Medicīna
Alerģisko reakciju ārstēšana, kontrole, profilakse un uzlabošana
Jaunu kaulu veidošanās veicināšana
Termiskās attēlveidošanas sistēmas, spektroskopija, teleskopi un eksimērlāzeri
Optisko komponentu, piemēram, logu un lēcu, ražošana
Izejviela/plašs pārraides gaismas frekvenču diapazons; zems refrakcijas indekss; augsta termostabilitāte
Citi
Metināšanas līdzekļu ražošana
Svarīgas sastāvdaļas metināšanas stieņu un metināšanas pulveru pārklājumos
Dehidratācijas un dehidrogenēšanas reakcija
Katalizators/paātrina reakcijas procesu
Bremžu uzliku ražošana
Piedeva/palīdz samazināt noberšanos, ko izraisa liels karstums un berze
|
| Ražošanas metode | Fluorīta atradnes, kas ir atrastas Ķīnā, galvenokārt tiek izmantotas raktuvēs, izmantojot pazemes ieguves metodi, vai seklās atklātās raktuvēs un pazemes dziļajās raktuvēs, rūdas korpusa visvairāk slīpajā dzīslā, arī paplašinājums ir liels. Kalnrūpniecības metode ir balstīta uz seklu caurumu saraušanās metodi. Ieguves procesā ir redzams "fosfāta iezis". Ražošanas metodēm parasti ir divi veidi: viena ir neapstrādāta rūda, kas var kļūt par kvalificētu rūdas koncentrātu, apstrādājot atlasīto rūdu, otrā ir ar rokām atlasīta liesa rūda un atliekas. |
| Apraksts | Kalcija fluorīds ir bezkrāsaina kristāliska vai balta pulverveida viela. Molekulmasa{{0}.08;Īpatnējais svars (H2O:1)=3.18 pie 20 grādiem ; Vārīšanās temperatūras =2495 grāds ; Sasalšanas/kušanas temperatūra=1423 grāds . Bīstamības identifikācija (pamatojoties uz NFPA-704 M vērtēšanas sistēmu): Veselība 2, Uzliesmojamība 0, Reaģētspēja 0. Ūdenī praktiski nešķīst. |
| Ķīmiskās īpašības | Kalcija fluorīds, CaF2, pazīstams arī kā fluorīts un laukšpats, ir bezkrāsaina cieta viela, kas sastāv no kubiskiem kristāliem. Tam ir zema šķīdība ūdenī, bet tas viegli šķīst amonija sāls šķīdumos. Kalcija fluorīdu izmanto fluorūdeņražskābes sintēzē un stikla kodināšanā. Kalcija fluorīds nav higroskopisks un ir samērā inerts. Tam ir pietiekami augsta izturība pret termiskiem un mehāniskiem triecieniem, un to ir viegli izgatavot dažādu ģeometriju detektoros. Kalcija fluorīdam ir ļoti zems tvaika spiediens, kas ļauj to izmantot dažādos vakuuma lietojumos. Tas nešķīst ūdenī un lielākajā daļā organisko šķīdinātāju, ļaujot radioaktīvos paraugus šķīdumā novietot tiešā saskarē ar kristālu. Kalcija fluorīds ir caurspīdīgs materiāls, ko izmanto staru noteikšanai līdz pat vairākiem simtiem keV un lādētu daļiņu noteikšanai. Tā zemā atomu skaita dēļ materiāla fotofrakcija ir salīdzinoši maza, kas ierobežo tā izmantošanu staru spektrometrijā pie lielākām enerģijām. Tomēr zemais atomu skaits padara kalcija fluorīdu par ideālu materiālu -daļiņu noteikšanai, jo ir neliels atpakaļizkliedes daudzums. |
| Fizikālās īpašības | Balts kubisks kristāls vai pulveris; refrakcijas indekss 1,434; blīvums 3,18 g/cm3; cietība 4 Moss; kūst pie 1418 grādiem; iztvaiko 2533 grādos; nešķīst ūdenī (16 mg/L pie 20 grādiem); Ksp 3,9 x10-11; nedaudz šķīst atšķaidītā minerālskābē; šķīst koncentrētās skābēs (ar reakciju). |
| Lietojumi | Dabā sastopamais CaF2 ir galvenais ūdeņraža fluorīda avots – plaša patēriņa ķīmiska viela, ko izmanto dažādu materiālu ražošanai. Fluorīds tiek atbrīvots no minerāla, iedarbojoties koncentrētai sērskābei: CaF2 (ciets)+H2SO4 (šķidrs) → CaSO4 (ciets)+2HF (gāze) CaF2 tiek izmantots kā optisks komponents, jo tā ķīmiskā stabilitāte nelabvēlīgos apstākļos. Kalcija fluorīdu parasti izmanto kā logu materiālu gan infrasarkanajiem, gan ultravioletajiem viļņu garumiem, jo tas ir caurspīdīgs šajos apgabalos (apmēram 0.15 līdz 9). mm) un tam ir ārkārtīgi zems refrakcijas indekss. Kalcija fluorīds ir ūdenī nešķīstošs kalcija avots izmantošanai pret skābekli jutīgos lietojumos, piemēram, metālu ražošanā. Īpaši zemās koncentrācijās (ppm) fluora savienojumus izmanto veselības jomā. Fluora savienojumiem ir arī ievērojams pielietojums sintētiskajā organiskajā ķīmijā. Tos parasti izmanto arī metālu leģēšanai un optiskai nogulsnēšanai. To izmanto arī kā plūsmu dzelzs, tērauda un to kompozītmateriālu kausēšanai un šķidrai apstrādei. Tās darbība ir balstīta uz tā kušanas temperatūru, kas ir līdzīga dzelzs kušanas temperatūrai, uz spēju šķīdināt oksīdus un uz spēju mitrināt oksīdus un metālus. |
| Lietojumi | Fluoršpats ir galvenais primārais fluora un tā savienojumu avots. Melnajā metalurģijā to izmanto kā plūsmu, lai palielinātu izdedžu plūstamību. Tērauda rūpniecība ir lielākais patērētājs; otrkārt ķīmiskā rūpniecība un trešais stikls un keramika. Sintētisko fluoršpatu izmanto optiskajā rūpniecībā (raida UV starus), un tīru kalcija fluorīdu izmanto kā katalizatoru dehidratācijā un dehidrogenācijā. Lieto dzeramā ūdens fluorēšanai. |
| Lietojumi | Kalcija fluorīds ir komerciāli svarīgs fluorīda savienojumu, kā arī ūdeņraža avots. Tas ir caurspīdīgs no ultravioletā līdz infrasarkanajam reģionam. To izmanto spektroskopijā, termiskās attēlveidošanas sistēmās un eksimēru lāzeros; to izmanto arī optisko komponentu, tostarp logu, prizmu un lēcu, ražošanā. Turklāt to izmanto arī alumīnija metalurģijā, bremžu uzliku ražošanas nozarēs un zobu emaljā. |
| Definīcija | Tīrs dabiski sastopams kalcija fluorīda veids. |
| Ražošanas metodes | Komerciālo produktu iegūst no dabā sastopama minerāla fluoršpata, kas ir attīrīts un pulverveida. To var arī nogulsnēt, sajaucot nātrija fluorīda šķīdumu ar šķīstošu kalcija sāli: Ca(NO3)2+ 2NaF → CaF2+ NaNO3 Alternatīvi, to var iegūt, apstrādājot kalcija karbonātu ar fluorūdeņražskābi:CaCO3+ 2HF → CaF2+ CO2 + H2O. |
| Definīcija | Kalcija fluorīda minerālu forma (CaF2), ko izmanto dažu cementu un stikla veidu ražošanā. |
| Vispārīgs apraksts | Pelēks pulveris vai granulas bez smaržas. Grimst ūdenī. |
| Reaktivitātes profils | Kalcija fluorīdam ir vāja oksidējošā vai reducējošā spēja. Tomēr redoksreakcijas joprojām var rasties. Lielākā daļa šīs klases savienojumu ir nedaudz šķīstoši vai nešķīstoši ūdenī. Ja šķīst ūdenī, tad šķīdumi parasti nav ne stipri skābi, ne stipri bāziski. Šie savienojumi nereaģē ar ūdeni. |
| Apdraudējums | Kairinošs līdzeklis. |
| Veselības apdraudējums | Maza akūta toksicitāte |
| Uzliesmojamība un sprādzienbīstamība | Nedegošs |
| Rūpnieciskai izmantošanai | Fluoršpats, ko sauc arī par fluorītu, ir kristālisks vai masīvs granulēts minerāls ar sastāvu CaF2, ko izmanto kā kušņu tērauda ražošanā, fluorūdeņražskābes ražošanā, opalescējošo stiklu ražošanā, keramikas emaljās, mākslīgā kriolīta iznīcināšanai, kā saistvielu stiklveida abrazīviem riteņiem un baltā cementa ražošanā. Tā ir labāka tērauda plūsma nekā kaļķakmens, veidojot šķidrus izdedžus un atbrīvojot dzelzi no sēra un fosfora. Skābes špals ir šķirne, ko izmanto fluorūdeņražskābes ražošanā. To izmanto arī aukstumaģentu, plastmasas un ķīmisko vielu ražošanai, kā arī alumīnija reducēšanai. Optiskais fluoršpats ir augstākā šķirne, taču tas nav izplatīts. Fluora kristāli optiskajām lēcām ir mākslīgi audzēti no skābes kvalitātes fluoršpata. Tīrs kalcija fluorīds, Ca2F6, ir bezkrāsains kristālisks pulveris, ko izmanto stikla kodināšanai, emaljās un berzes samazināšanai mašīnu gultņos. To izmanto arī keramikas daļām, kas ir izturīgas pret fluorūdeņražskābi un lielāko daļu citu skābju. Kalcija fluorīta molekulā ir silīcijs, un tas ir kristālisks pulveris, ko izmanto emaljām. Dzidrie rombveida fluorīda kristāli, ko izmanto elektriskās enerģijas pārveidošanai gaismā, ir svina fluorīds, PbF2. |
| Drošības profils | Vidēji toksisks intraperitoneāli. Viegli toksisks norijot. Eksperimentāls teratogēns. Citi eksperimentāli reproduktīvie efekti. Ziņots par mutāciju datiem. Skatiet arī FLUORĪDI un KALCIJA SAVIENOJUMI. Karsējot līdz sadalīšanai, tas izdala toksiskus F- izgarojumus. |
| Iespējama iedarbība | Kalcija fluorīdu izmanto fluorūdeņražskābes ražošanai; kā plūsma tērauda ražošanā; kausēšanā; elektriskā loka metināšana, stikla un keramikas izgatavošana; un fluorizēt dzeramo ūdeni. |
| Pirmā palīdzība | Ja šī ķīmiskā viela nokļūst acīs, nekavējoties izņemiet visas kontaktlēcas un nekavējoties skalojiet vismaz 15 minūtes, laiku pa laikam paceļot augšējo un apakšējo plakstiņu. Nekavējoties meklējiet medicīnisko palīdzību. Ja šī ķīmiskā viela nonāk saskarē ar ādu, novelciet piesārņoto apģērbu un nekavējoties nomazgājiet ar ziepēm un ūdeni. Nekavējoties meklēt medicīnisko palīdzību. Ja šī ķīmiskā viela ir ieelpota, noņemiet no iedarbības, sāciet glābšanas elpošanu (izmantojot vispārējus piesardzības pasākumus, tostarp reanimācijas masku), ja elpošana ir apstājusies, un CPR, ja sirds darbība ir apstājusies. Nekavējoties nogādāt medicīnas iestādē. Kad šī ķīmiskā viela ir norīta, meklējiet medicīnisko palīdzību. Ārsts vai pilnvarots feldšeris var apsvērt alumīnija hidroksīda gela ievadīšanu, ja tas ir pie samaņas. |
| uzglabāšana | Krāsas kods-Zaļš: Var izmantot vispārīgu uzglabāšanu. Uzglabāt cieši noslēgtos traukos vēsā, labi vēdināmā vietā, prom no skābēm un ķīmiski aktīviem metāliem (piemēram, kālija, nātrija, magnija un cinka), jo radīsies kodīgs fluorūdeņradis. |
| Piegāde | Kalcija fluorīds nav īpaši ietverts DOT savos uz veiktspēju orientētajos iepakojuma standartos. |
| Nesaderības | Putekļi var veidot sprādzienbīstamu maisījumu ar gaisu. Reaģē ar ūdeni, mitru gaisu un tvaiku, izdalot uzliesmojošu ūdeņraža gāzi; un gaisā var pašaizdegties. Spēcīgs reducētājs; nesaderīgs ar oksidētājiem (hlorāti, nitrāti, peroksīdi, permanganāti, perhlorāti, hlors, broms, fluors utt.); saskare var izraisīt aizdegšanos vai sprādzienu. Sargāt no sārmainiem materiāliem, stiprām bāzēm, stiprām skābēm, oksoskābēm, epoksīdiem. Nesaderīgs ar metālu halogenātiem, sudraba fluorīdu un tetrahidrofurānu |
| Kalcija fluorīda preparāti un izejvielas |
| Izejvielas | Hydrogen fluoride-->Calcium hydroxide-->CARBON MONOXIDE-->Quartz-->Calcium acetate-->kalcija magnija fosfāts (CMP) |
| Sagatavošanas produkti | Hydrogen fluoride-->Boron trifluoride diethyl etherate-->Potassium Phosphate Monobasic-->Hexafluorosilicic acid-->Calcium cyanamide-->Sodium fluoride-->Trisodium hexafluoroaluminate-->Aluminum fluoride-->bastnasite-->Carbon tetrafluoride-->cryolite-->ZINC SILICOFLUORIDE-->MAGNIJA HEKSAFLUORACETILACETONĀTA DIHIDRĀTS |
Populāri tagi: kalcija fluorīds, Ķīnas kalcija fluorīda ražotāji, piegādātāji, rūpnīca
Pāri: Cinka fluorīds
Nākamo: Stroncija fluorīds
Jums varētu patikt arī
Nosūtīt pieprasījumu


