| Ķīmiskās īpašības |
bēšs ciets |
| Ķīmiskās īpašības |
Ciānpiridīni ir šādi: 2-ciano-: balts līdz dzeltenbrūns šķidrums vai cieta viela. Mandeļu smarža. Vārīšanās temperatūra =2213 grāds ; sasalšanas/kušanas temperatūras=27 grāds ; uzliesmošanas temperatūra=89 grāds . 3-ciān-: bezkrāsains šķidrums vai pelēka kristāliska cieta viela. |
| Lietojumi |
4-Cianopiridīnu izmanto kā starpproduktu organiskajā sintēzē un farmaceitiskās vielas, piemēram, izonikotinilhidrazīdu, ko izmanto tuberkulozes ārstēšanā. To izmanto kā prekursoru izonikotīnskābes un 4-diemtilaminopiridīna (DMAP) pagatavošanai. Tas ir iesaistīts 6-metil-2-piridin-4-il-pirimidin-4-ilamīna sintēzē, reaģējot ar acetonitrilu. |
| Sintēze |
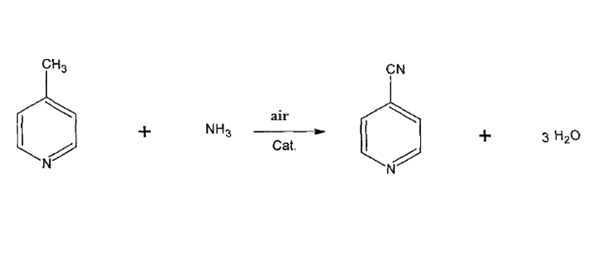
4-Cianopiridīns tiek sintezēts, 4-metilpiridīnam reaģējot ar amonjaku un gaisu katalizatora klātbūtnē. Konkrētie sintēzes posmi ir šādi:
{{0}}Metilpiridīna un amonjaka iztvaicēšanas priekšsildīšana līdz 180-330 grādiem, pēc tam maisīšanas tvertnē un gaisa vienmērīga sajaukšana, fiksētā slāņa reaktorā pa fiksētā slāņa reaktora augšpusi pēc sadales ar katalizatoru pildītā reaktora reakcijas temperatūras kontrole ir 330-450 grādu C diapazonā, reakcijas galvas spiediens tiek kontrolēts diapazonā no 0.020-0,070 KPa, reakcijas temperatūra ir ko kontrolē kausēti sāļi, reakcijas gāze pēc reakcijas beigām Pēc reakcijas reakcijas gāze tika kondensēta līdz mīnus nulles frakcionēšanai, lai iegūtu 4-ciānpiridīna kopproduktu, un jēlprodukts tika destilēts, lai iegūtu gatavais 4-cianopiridīna produkts. 4-metilpiridīna konversijas līmenis bija virs 99%, un 4-ciānpiridīna iznākums pārsniedza 98%.
 |
| Iespējama iedarbība |
Ierobežojumi gaisā NIOSH IDLH525 mg/m3 NIOSH REL: (nitrili) 2 ppm, griestu koncentrācija, nedrīkst pārsniegt nevienā 15-minūtes darba periodā. |
| Piegāde |
UN3276 Nitrili, šķidri, toksiski, nos, bīstamības klase: 6.1; Etiķetes: 6.1-Indīgi materiāli, nepieciešams tehniskais nosaukums, iespējama ieelpošanas bīstamība (5. īpašais noteikums). |
| Nesaderības |
Oksidētāji, piemēram, perhlorāti, peroksīdi un permanganāti. Nitrili var polimerizēties metālu un dažu metālu savienojumu klātbūtnē. Tie nav saderīgi ar skābēm; nitrilu sajaukšana ar spēcīgām oksidējošām skābēm var izraisīt ārkārtīgi spēcīgas reakcijas. Nitrili parasti nav saderīgi ar citiem oksidētājiem, piemēram, peroksīdiem un epoksīdiem. Bāzu un nitrilu kombinācija var radīt ūdeņraža cianīdu. Nitrilus hidrolizē gan skābē, gan bāzē, iegūstot karbonskābes (vai karbonskābju sāļus). Šīs reakcijas rada siltumu. Peroksīdi pārvērš nitrilus par amīdiem. Nitrili var enerģiski reaģēt ar reducētājiem. Acetonitrils un propionitrils šķīst ūdenī, bet nitriliem, kas ir augstāki par propionitrilu, ir zema šķīdība ūdenī. Tie nešķīst arī ūdens skābēs. |




![9-[(2-Acetoksietoksi)metil]-N2-acetilguanīns](/uploads/41226/small/9-2-acetoxyethoxy-methyl-n2-acetylguaninec7eaf.jpg?size=336x0)




