
Produkta ievads
| Tetrametilamonija hlorīds Pamatinformācija |
| Organiskās sintēzes katalizators Tetrametilamonija hidroksīda elektrolītiskā sagatavošana PHBHQ tipa termoreaktīvo šķidro kristālisko epoksīdsveķu (LCER) sagatavošana Lietošanas veidi |
| Produkta nosaukums: | Tetrametilamonija hlorīds |
| Sinonīmi: | Amonijs, tetrametil-, hlorīds;Metānamīns, N,N,N-trimetil-, hlorīds;TETRAMETYLAMMONIUM HLORIDETETRAMETHYLAMMONIUM HLORIDETETRAMETHYLAMMONIUM HLOrīds ide;tetrametils -amonihlorīds;tetramīnhlorīds;USAF AN-8 |
| CAS: | 75-57-0 |
| MF: | C4H12ClN |
| MW: | 109.6 |
| EINECS: | 200-880-8 |
| Produktu kategorijas: | Amonija hlorīdi (kvartāri); kvartāra amonija savienojumi; kvartāra amonija sāļi; amonija sāļiNukleīnskābes noteikšana un hibridizācija; farmaceitiskie starpprodukti; smalkās ķīmiskās vielas; zaļākas alternatīvas: katalīze; hibridizācijas komplekti un reaģenti; hibridizācijas komplekti; sāls;bc0001 ;75-57-0 |
| Mol fails: | 75-57-0.mol |
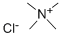 |
|
| Tetrametilamonija hlorīda ķīmiskās īpašības |
| Kušanas punkts | >300 grādi (lit.) |
| Vārīšanās punkts | 165,26 grādi (aptuvens aprēķins) |
| blīvums | 1 % 2C17 G/CM3 |
| refrakcijas indekss | 1,5320 (aptuvens) |
| uzglabāšanas temp. | Uzglabāt zem +30 grādu. |
| šķīdība | metanols: 0,1 g/mL, dzidrs, bezkrāsains |
| formā | Higroskopisks kristālisks pulveris |
| Īpaša gravitāte | 1.169 |
| krāsa | Balta līdz ziloņkaula krāsai |
| PH | 6-8 (100 g/l, H2O, 20 grādi) |
| Smarža | Bez smaržas |
| PH diapazons | 6 - 8 |
| Šķīdība ūdenī | >60 g/100 ml (20 ºC) |
| Jūtīgs | Higroskopisks |
| λmaks | λ: 260 nm Maksimālais: 0,02 λ: 280 nm Maksimālais: 0,02 |
| BRN | 2496575 |
| Stabilitāte: | Stabils. Nesaderīgs ar spēcīgiem oksidētājiem, ūdeni. Higroskopisks. |
| CAS datu bāzes atsauce | 75-57-0(CAS datu bāzes atsauce) |
| NIST ķīmijas atsauce | Tetrametilamonija hlorīds (75-57-0) |
| EPA vielu reģistra sistēma | Tetrametilamonija hlorīds (75-57-0) |
| Drošības informācija |
| Bīstamības kodi | T,Xn |
| Riska paziņojumi | 21-25-36/37/38-20/21/22 |
| Drošības paziņojumi | 26-36/37-45-37/39-28A-28-36 |
| RIDADR | ANO 2811 6.1/PG 2 |
| WGK Vācija | 1 |
| RTECS | BS7700000 |
| F | 3-10 |
| TSCA | Jā |
| Bīstamības klase | 6.1 |
| Iepakojuma grupa | II |
| HS kods | 29239000 |
| Dati par bīstamām vielām | 75-57-0(Dati par bīstamām vielām) |
| Toksiskums | LD50 iekšķīgi trušiem: 50 mg/kg LD50 dermāli žurkām 537 mg/kg |
| MSDS informācija |
| Pakalpojumu sniedzējs | Valoda |
|---|---|
| N,N,N-trimetilmetānamīna hlorīds | Angļu |
| SigmaAldrihs | Angļu |
| ACROS | Angļu |
| ALFA | Angļu |
| Tetrametilamonija hlorīda lietošana un sintēze |
| Organiskās sintēzes katalizators | Tetrametilamonija hlorīds ir fāzes pārneses katalizators organiskās sintēzes fāzē, un tā katalītiskā aktivitāte ir spēcīgāka nekā trifenilfosfīns un trietilamīns. Istabas temperatūrā tas ir balts kristālisks pulveris, gaistošs, kairinošs un viegli uzsūcošs mitrums. Tas viegli šķīst metanolā, šķīst ūdenī un karstā etanolā, bet nešķīst ēterī un hloroformā. Karsējot līdz virs 230 grādiem, tā sadalās trimetilamīnā un metilhlorīdā. Vidējā letālā deva (pelēm, intraperitoneāli) ir aptuveni 25 mg/kg. To izmanto arī šķidro kristālu epoksīda savienojumu sintēzei un Pope un polarogrāfiskajai analīzei, kā arī elektroniskajai rūpniecībai. Iepriekš minētā informācija ir rediģēta Dai Xiongfeng ķīmiskajā grāmatā. |
| Tetrametilamonija hidroksīda elektrolītiskā sagatavošana | Tetrametilamonija hidroksīds ir sava veida organiskā bāze, un tam ir plašs pielietojums gan rūpniecībā, gan zinātniskajā pētniecībā. Mūsu valstī to galvenokārt izmanto kā katalizatoru organisko silīcija produktu, piemēram, sintētiskās silikona eļļas, silikona gumijas un silikona sveķu, sintēzē. Lai gan tam ir mazs lietošanas apjoms, tas var būtiski ietekmēt gan produkta ražu, gan kvalitāti. Ārzemēs to galvenokārt izmanto poliesteru bāzes polimēriem, tekstilizstrādājumiem, plastmasām, pārtikai, ādai, kokapstrādei, galvanizācijai un dažu veidu mikroorganismiem. Tagad tetrametilamonija hidroksīds ir ienācis progresīvo tehnoloģiju jomās. Piemēram, elektronisko shēmu un mikroskopisko lokšņu ražošanas ražošanas nozarē to var izmantot kā integrētās shēmas plates tīrīšanas līdzekli, kā arī Si-SiO2 saskarnes anizotropos korozīvos līdzekļus pusvadītāju mikrofabrikas tehnikā. Attīstoties zinātnei un tehnoloģijām, pieaug arī prasības šāda veida ķīmiskajām vielām, izvirzot augstākas prasības gan tetrametilamonija hidroksīda kvalitātei, gan kvantitātei. Elektrolītiskās metodes izmantošanas pamatprincips tetrametilamonija hidroksīda pagatavošanai ir tāds, ka tetrametilamonija hlorīda ūdens šķīdumam elektrolītiskās vannas anoda nodalījumā elektriskā spēka ietekmē hlorīda joni migrē anoda virzienā līdz izlādei. anods rodas, lai radītu hloru. Tikmēr jonu apmaiņas membrānas selektīvās caurlaidības dēļ hlorīds difūzijas ceļā nevar iekļūt caur jonu apmaiņas membrānu. Tā vietā tikai tetrametilamonija joni var selektīvi iekļūt katoda nodalījumā un tur bagātināties. Ūdens molekula elektrolizatora katoda kamerā sadalās ūdeņraža un hidroksiljonos. Pēdējais precīzi saistās ar tetrametilamonija joniem, kas migrē no anoda kameras, veidojot tetrametilamonija hidroksīdu. Palielinoties elektrībai, tetrametilamonija hidroksīda koncentrācija turpina uzlaboties, beidzot sasniedzot vēlamo jēlnaftas galīgo koncentrāciju. Anodiskā elektroķīmiskā reakcija ir: (CH3) 4NCl → (CH3) 4N ++ Clˉ2Clˉ-2 e → Cl2 ↑ Katodiskā elektroķīmiskā reakcija ir: H2O → H + + OHˉ (CH3) 4N ++ OHˉ → (CH3) 4NOH 2H ++ 2e → H2 ↑ Kopējā reakcija ir: 2 (CH3) 4NCl + 2H2O → 2 (CH3) 4NOH + H2 ↑ + Cl2 ↑ Ūdeņradis, kas rodas elektrolīzes laikā, tiek izvadīts ar iegūto hloru, ko absorbē sārmains šķīdums, lai iegūtu nātrija hipohlorītu, kas ir galvenais balinātāja ražošanas izejmateriāls. Tāpēc šī tetrametilamonija hidroksīda iegūšanas metode ir vienkārša ar augstu tīrības pakāpi un neizraisa vides piesārņojumu. |
| PHBHQ tipa termoreaktīvo šķidro kristālisko epoksīda sveķu (LCER) sagatavošana | Kā šķīdinātāju izmantot toluolu, kā katalizatoru koncentrētu sērskābi un borskābi, trīskakla kolbā pievienot vienādu daudzumu hidroksibenzoskābes un 1,4-hidrohinona, 6 stundas reaģēt 120-130 grādu temperatūrā; pēc atdzesēšanas atkārtoti mazgā ar destilētu ūdeni un iegūst p-hidroksibenzoskābes p-hidrohinona esteri pēc žāvēšanas vakuumā (balta cieta viela, iznākums 87,5%). Iepriekš minēto produktu izšķīdina pārmērīgā epihlorhidrīna daudzumā, pievieno tetrametilamonija hlorīdu un 10 stundas ļaujiet reaģēt 60-70 grādu temperatūrā; pa pilienam pievieno lieko 45% NaOH ūdens šķīduma daudzumu (pievienošana aizņem 6 h). Epihlorhidrīna pārpalikums tika destilēts pazeminātā spiedienā; reakcijas maisījumu mazgā ar acetona-metanola maisījumu kristalizācijai; to tālāk pakļauj vakuuma žāvēšanai, lai iegūtu baltus PHBHQ tipa termoreaktīvus šķidros kristāliskos epoksīda sveķus (ar iznākumu 37,5%). Sajauc PHBHQ un cietinātāju stehiometriski karsēšanai un kausēšanai, liešanai ar cietēšanas procesu 90 grādi × 1 h; 120 grādi × 2h; 150 grādi × 2h; 180 grādi × 2h. |
| Lietojumi | 1. To var izmantot kā polarogrāfiskās analīzes reaģentus, ko plaši izmanto elektronikas rūpniecībā. 2. Tetrametilamonija hlorīds ir fāzes pārneses katalizators organiskajā sintēzē, un tā katalītiskā aktivitāte ir spēcīgāka nekā trifenilfosfīns un trietilamīns. Istabas temperatūrā tas ir balts kristālisks pulveris, gaistošs, kairinošs un viegli uzsūcošs mitrums. Tas viegli šķīst metanolā, šķīst ūdenī un karstā etanolā, bet nešķīst ēterī un hloroformā. Karsējot līdz virs 230 grādiem, tā sadalās trimetilamīnā un metilhlorīdā. Vidējā letālā deva (pelēm, intraperitoneāli) ir aptuveni 25 mg/kg. To izmanto arī šķidro kristālu epoksīda savienojumu sintēzei un Pope un polarogrāfiskajai analīzei, kā arī elektroniskajai rūpniecībai. |
| Ķīmiskās īpašības | balti kristāli |
| Lietojumi | Ķīmiskais starpprodukts, katalizators, inhibitors. |
| Lietojumi | Tetrametilamonija hlorīds kopā arN-hidroksiftalimīdu un ksantonu var izmantot kā efektīvu hlorīda katalītisko sistēmu ogļūdeņražu aerobai oksidēšanai, veidojot atbilstošos skābekļa savienojumus. To var izmantot arī kā fāzes pārneses katalizatoru arilfluorīdu sintēzei, izmantojot aktivētu arilhlorīdu selektīvās hlorīda/fluorīda apmaiņas reakciju ar kālija fluorīdu cietā-šķidrā fāzē. |
| Lietojumi | TMAC var izmantot jonu apmaiņas procedūrās, lai parādītu pH pieaugumu, lai izprastu katalizatora [CTA]Si-MCM-41 ķīmisko uzvedību, izmantojot Knoevenagel kondensācijas modeli. |
| Definīcija | ChEBI: N,N,N-trimetilmetānamīna hlorīds ir organiska molekulāra vienība. |
| Vispārīgs apraksts | Tetrametilamonija hlorīds ir kvaternārais amonija sāls, ko parasti izmanto kā katalizatoru tā termiskās stabilitātes un arī tolerances pret spēcīgām ūdens bāzēm vai nukleofīliem dēļ. |
| Drošības profils | Saindē, norijot, intraperitoneāli un subkutāni. Karsējot līdz sadalīšanai, tas izdala ļoti toksiskus NOx, NH3 un Cl- dūmus. Skatīt arī HLORĪDI. |
| Attīrīšanas metodes | Kristalizējiet hlorīdu no EtOH, EtOH/CHCl3, EtOH/dietilētera, acetona/EtOH (1:1), izopropanola vai ūdens. Brīvā amīna pēdas var noņemt, mazgājot ar CHCl3. [Beilstein 4 IV 145.] |
| Tetrametilamonija hlorīda sagatavošanas produkti un izejvielas |
| Izejvielas | Tetramethylammonium hydroxide-->Sodium hydride-->Trimethylamine-->Trimetilamīna hidrohlorīds |
| Sagatavošanas produkti | 2,6-DICHLORO-4-ISOCYANATOPYRIDINE-->4-FLUORO-2-NITROBENZONITRILE-->2-Hydroxyethyl methacrylate-->:2-Isopropyl-5-methylanisole-->3-PYRIDINEMETHANOL N-OXIDE-->4-Phenylpyridine-N-oxide-->m-anizilspirts |
Populāri tagi: tetrametilamonija hlorīds, Ķīnas tetrametilamonija hlorīda ražotāji, piegādātāji, rūpnīca
Nākamo: Tetraetilamonija hlorīds
Jums varētu patikt arī
Nosūtīt pieprasījumu





![1-(4-hlorfenil)-3-[(2-nitrofenil)metoksi]-1H-pirazols](/uploads/41226/small/1-4-chlorophenyl-3-2-nitrophenyl-methoxy-1he4202.jpg?size=336x0)

